题目内容
(10分)完成下列化学方程式或离子方程式。
①.过氧化钠与二氧化碳反应化学方程式:
②.铝和NaOH溶液反应化学方程式:
③.氢氧化铝和NaOH溶液反应离子方程式:
④.硫酸亚铁与氢氧化钠溶液离子方程式:
⑤.FeCl3和Cu反应离子方程式:
①. 2Na2O2 + 2CO2 = 2Na2CO3 +O2↑ ;②.2Al+2NaOH+2H2O=2NaAlO2+3H2↑
③. Al(OH)3 +OH- = AlO2-+2H2O ;④.Fe2++2OH-= Fe(OH)2↓.
⑤. 2Fe3++Cu=2Fe2++Cu2+
【解析】
试题分析:书写离子方程式,只有可溶性强电解质写成离子,单质、氧化物、气体、沉淀、弱电解质不能拆写为离子,①过氧化钠与二氧化碳反应化学方程式2Na2O2 + 2CO2 = 2Na2CO3 +O2↑;②.铝和NaOH溶液反应化学方程式2Al+2NaOH+2H2O=2NaAlO2+3H2↑;③.氢氧化铝和NaOH溶液反应离子方程式Al(OH)3 +OH- = AlO2-+2H2O;④.硫酸亚铁与氢氧化钠溶液离子方程式Fe2++2OH-= Fe(OH)2↓;⑤.FeCl3和Cu反应离子方程式2Fe3++Cu=2Fe2++Cu2+。
考点:本题考查离子方程式书写。

 中考解读考点精练系列答案
中考解读考点精练系列答案下列各组物质中,X是主体物质,Y是少量杂质,Z是要除去杂质而加入的试剂,其中正确的组别是
X | Y | Z | |
A. | FeCl2溶液 | FeCl3 | KSCN溶液 |
B. | Fe粉 | A1粉 | 稀盐酸 |
C. | Fe2(SO4)3溶液 | FeS04 | C12 |
D. | FeCl2溶液 | CuCl2 | Fe粉 |
相同温度下,根据三种酸的电离平衡常数,下列判断正确的是
酸 | HX | HY | HZ |
Ka/mol·L-1 | 9×10-7 | 9×10-6 | 2×10-2 |
A.三种酸的强弱关系: HX>HY>HZ
B.反应 HZ+Y-===HY+Z-能够发生
C.相同温度下,0.1 mol?L?1的NaX、NaY、NaZ溶液,NaZ溶液pH最大
D.相同温度下,1 mol?L?1HX溶液的电离常数大于0.1 mol?L?1HX
 2R(g),由图分析y所表示的量以及反应的能量变化为(图中压强P1>P2>P3)
2R(g),由图分析y所表示的量以及反应的能量变化为(图中压强P1>P2>P3)
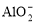 B.Cu2+ C.Al3+ D.Mg2+
B.Cu2+ C.Al3+ D.Mg2+