题目内容
16.同温同压下,影响气体体积大小的主要因素是( )| A. | 气体分子间平均距离 | B. | 气体分子数目 | ||
| C. | 气体分子本身的体积 | D. | 气体相对分子质量 |
分析 由于气体的分子间距离远大于分子本身大小,则决定气体体积的因素主要是气体的分子数目和分子间距离;在同温同压下,气体的分子之间的距离基本相等,所以决定气体体积的是气体的分子数或物质的量,以此进行解答.
解答 解:气体的分子间距离远大于分子本身大小,决定气体体积的因素主要是气体的分子数目以及分子间距离,而同温同压下,气体分子间的平均距离一定时,气体物质的量的多少决定气体的体积大小,而与气体分子的直径、气体分子的式量无关,
故选B.
点评 本题考查阿伏伽德罗定律及其应用,题目难度中等,试题侧重于学生的分析能力的考查,注意明确影响气体体积的因素-气体的分子数目和分子间距离.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
6.下列装置或操作正确且能达到实验目的是( )
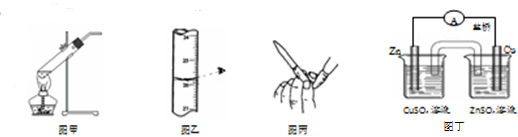

| A. | 用图甲所示装置加热分解NaHCO3固体 | |
| B. | 用图乙所示读取滴定管读数 | |
| C. | 用图丙所示排碱式滴定管尖嘴内的气泡 | |
| D. | 用图丁所示装置构成铜锌原电池 |
4.下列化学式只能表示一种物质的是( )
| A. | CH2Cl2 | B. | C2H4Cl2 | C. | C4H5 | D. | C5H12 |
11.浩瀚的海洋中蕴藏着丰富的资源,海水中含量最多的氯化物是( )
| A. | NaCl | B. | MgCl2 | C. | KCl | D. | CaCl2 |
1.相同质量的Na、Mg、Al分别与足量盐酸充分反应,生成氢气的质量比为( )
| A. | 1:2:3 | B. | 23:24:37 | C. | 23:12:9 | D. | 36:69:92 |
8.某课题小组研究“铁及其化合物性质”时,向 FeSO4 溶液中滴加少量KSCN溶液,无明显现象.再滴加 H2 O2 溶液时,发现:随着H 2O 2量的增加,溶液先变红,后褪色,并有气泡产生.为弄清楚产生这种异常现象的原因,他们进行了如下探究.
[提出假设]
假设一:产生的气体可能是O 2.
假设二:产生的气体可能是N2、SO 2、CO 2 等气体.
(1 )请写出H2O 2氧化FeSO4的离子方程式2Fe2++H2O2+2H+=2Fe3++2H2O.
[实验设计]
为验证假设二是否成立,课题小组设计如下实验来验证气体成分.
所用试剂:H 2 O2 溶液、FeCl 2 溶液、KSCN 溶液、品红溶液、酸性高锰酸钾溶液、澄清石灰水、NaOH 溶液等.
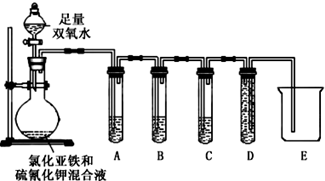
请完成下表中的内容:
[思考与交流]
(4 )根据题目中所给的信息及实验推断出物质还原性的强弱顺序:Fe2+>SCN-(填“>”或“<”),理由是向FeCl2和KSCN混合液中加入少量双氧水,溶液先变红,说明双氧水优先氧化Fe2+.
(5 )有同学认为:KSCN 被氧化的产物中可能还含有 SO 42-,请设计一个简单实验验证.
[提出假设]
假设一:产生的气体可能是O 2.
假设二:产生的气体可能是N2、SO 2、CO 2 等气体.
(1 )请写出H2O 2氧化FeSO4的离子方程式2Fe2++H2O2+2H+=2Fe3++2H2O.
[实验设计]
为验证假设二是否成立,课题小组设计如下实验来验证气体成分.
所用试剂:H 2 O2 溶液、FeCl 2 溶液、KSCN 溶液、品红溶液、酸性高锰酸钾溶液、澄清石灰水、NaOH 溶液等.

请完成下表中的内容:
| 实验过程和现象 | 结论 |
| (2)试管A中盛有品红溶液现象:品红溶液褪色 | 证明气体中含有SO2 |
| (3)试管B中现象紫色酸性高锰酸钾溶液颜色不变或变浅试管C中现象:澄清石灰水变浑浊 | 证明气体中含有CO2 |
(4 )根据题目中所给的信息及实验推断出物质还原性的强弱顺序:Fe2+>SCN-(填“>”或“<”),理由是向FeCl2和KSCN混合液中加入少量双氧水,溶液先变红,说明双氧水优先氧化Fe2+.
(5 )有同学认为:KSCN 被氧化的产物中可能还含有 SO 42-,请设计一个简单实验验证.
| 实验过程 | 实验现象及结论 |
 已知:H2S在高温下分解生成硫蒸气和H2.现测得某温度下,H2S分解过程中各物质的物质的量随时间变化关系如图所示,则生成的硫蒸气化学式为( )
已知:H2S在高温下分解生成硫蒸气和H2.现测得某温度下,H2S分解过程中各物质的物质的量随时间变化关系如图所示,则生成的硫蒸气化学式为( )