题目内容
1.某化学兴趣小组为探究铜跟浓硫酸的反应,用如图所示装置进行有关实验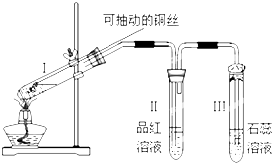
请回答下列问题:
(1)写出试管Ⅰ中发生反应的化学方程式并标出电子转移的方向和数目为
 .
.(2)铜丝可抽动的作用是抽动铜丝,以随时中止反应.
(3)试管Ⅱ中现象为品红溶液褪色,可证明SO2具有漂白性;试管Ⅲ中现象为石蕊溶液显红色.
(4)试管Ⅲ的管口用浸有碱(NaOH溶液)的棉团塞住,其作用是吸收SO2气体,防止空气污染; 发生反应的化学方程式为SO2+2NaOH=Na2SO3+H2O.
分析 (1)试管Ⅰ中铜与浓硫酸在加热条件下反应生成硫酸铜、二氧化硫气体和水,根据化合价变化分析电子转移情况,然后用单线桥标出电子转移的方向和数目;
(2)通过抽动铜丝可以控制反应的停止;
(3)试管Ⅱ中装有品红溶液,二氧化硫具有漂白性,能够使品红溶液褪色;二氧化硫溶液显示酸性,所以试管Ⅲ中石蕊试液变红;
(4)二氧化硫为污染气体,需要用氢氧化钠溶液吸收多余的二氧化硫;二氧化硫与氢氧化钠溶液反应生成亚硫酸钠和水.
解答 解:(1)试管Ⅰ中铜与浓硫酸在加热条件下反应生成二氧化硫,反应的化学方程式为:Cu+2H2SO4(浓)$\frac{\underline{\;△\;}}{\;}$CuSO4+SO2↑+2H2O,该反应中铜失去2个,二氧化硫中S原子得到2个电子,用单线桥标出电子转移的方向和数目为 ,
,
故答案为: ;
;
(2)通过抽动铜丝,以随时中止反应,避免浪费原料、减少污染气体的产生,
故答案为:抽动铜丝,以随时中止反应;
(3)二氧化硫具有漂白性,所以试管Ⅱ中品红溶液褪色;二氧化硫为酸性氧化物,能够与水反应生成亚硫酸,所以试管Ⅲ中的石蕊溶液显红色,证明了二氧化硫的水溶液显示酸性,
故答案为:品红溶液褪色;漂白;石蕊溶液显红色;
(4)二氧化硫有毒,多余的气体不能直接排放,需要用氢氧化钠溶液吸收SO2气体,防止空气污染,反应的化学方程式为:SO2+2NaOH=Na2SO3+H2O,
故答案为:吸收SO2气体,防止空气污染;SO2+2NaOH=Na2SO3+H2O.
点评 本题考查了浓硫酸的化学性质,题目难度中等,注意掌握铜与浓硫酸的反应原理,明确二氧化硫的性质及检验方法,试题侧重基础知识的考查,培养了学生的化学实验能力.

练习册系列答案
相关题目
14.下列叙述中,不属于核外电子的特点的是( )
| A. | 质量很小 | B. | 运动范围很小 | ||
| C. | 运动速率很快 | D. | 有确定的运动轨道 |
12.关于实现下列物品用途的主要物质的说法,不正确的是( )
| A. | 硫酸是铅蓄电池的电解质溶液,铅蓄电池可实现化学能转变成电能 | |
| B. | 硅酸干凝胶是硅酸干燥剂的主要成分,作用是吸收水分 | |
| C. | 肥皂的主要成分是硬脂酸钠,可以用于除去油污 | |
| D. | 二氧化硅是光能转化为电能的转化材料 |
6.金属材料是使用最广泛的一种材料,从古代到现代,金属材料经历了几次较大的变革.请回答下列问题:
(1)下面表格中的数据(铁和铜的某些物理数据)摘自某化学手册.
由表可推知,人类最早使用的金属材料是铜,请写出判断的理由:铜的熔点低于铁的熔点.
(2)考古中出土的青铜器、铁剑等往往锈迹斑斑.请完成下面铜、铁制品在自然条件下发生锈蚀的化学方程式:
①□Cu+□O2+□H2O+□CO2═□Cu2(OH)2CO3
②□Fe+□O2+□H2O═□Fe2O3•nH2O
(3)镁、铝是现代人常用的金属材料,这些活泼金属的冶炼方法是电解法,工业生产中,镁的冶炼采用的反应物是熔融氯化镁(或MgCl2),铝的冶炼采用的反应物是熔融氧化铝(或Al2O3).
(1)下面表格中的数据(铁和铜的某些物理数据)摘自某化学手册.
| 金属 | 颜色 | 密度(g/cm3) | 熔点(℃) | 沸点(℃) | 比热[KJ/kg•℃] |
| Fe | 银白色 | 7.86 | 1 535 | 2 750 | 0.44 |
| Cu | 红色 | 8.92 | 1 083 | 2 567 | 0.38 |
(2)考古中出土的青铜器、铁剑等往往锈迹斑斑.请完成下面铜、铁制品在自然条件下发生锈蚀的化学方程式:
①□Cu+□O2+□H2O+□CO2═□Cu2(OH)2CO3
②□Fe+□O2+□H2O═□Fe2O3•nH2O
(3)镁、铝是现代人常用的金属材料,这些活泼金属的冶炼方法是电解法,工业生产中,镁的冶炼采用的反应物是熔融氯化镁(或MgCl2),铝的冶炼采用的反应物是熔融氧化铝(或Al2O3).
11.下列文字表述与反应方程式对应且正确的是( )
| A. | 甲烷与氯气反应:CH4+4Cl2→CCl4+4HCl | |
| B. | 用醋酸除去水垢:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| C. | 乙醇和钠反应:2CH3CH2OH+2Na→2CH3CH2ONa+H2↑ | |
| D. | 苯和浓硝酸、浓硫酸的混合物水浴60℃反应: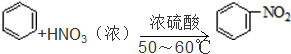 |

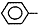 CH=CH2),聚苯乙烯的化学式为
CH=CH2),聚苯乙烯的化学式为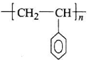 .
.