题目内容
在铜锌原电池中,锌电极上发生的反应为Zn-2e-=Zn2+,则( )
| A、锌电极为负极 |
| B、锌电极为正极 |
| C、反应中Zn被氧化 |
| D、反应中Zn被还原 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:在原电池中,失电子的金属作负极,失电子的物质发生氧化反应而作还原剂,得电子的物质发生还原反应而作氧化剂,氧化剂被还原,还原剂被氧化.
解答:
解:锌失电子发生氧化反应而作负极,铜作正极,在该反应中锌作还原剂,还原剂被氧化,故选AC.
点评:本题考查了原电池原理,根据得失电子及反应类型来确定正负极,注意不能根据金属的活泼性强弱确定正负极,要根据得失电子难易程度确定正负极,题目难度不大.

练习册系列答案
相关题目
通过复习总结,你认为下列对化学知识的理解不合理的是( )
| A、盛放氢氧化钠溶液的试剂瓶用橡皮塞,不用玻璃塞 |
| B、常温下可用铁、铝制容器盛放浓硫酸或浓硝酸,因为它们不反应 |
| C、N2和H2合成NH3,属于氮的固定 |
| D、丁达尔效应是检验胶体和溶液的一种常用方法 |
NO和CO都是汽车尾气里的有害物质,它们能缓慢反应,生成氮气和二氧化碳,对此反应,下列叙述正确的是( )
| A、使用催化剂不改变反应速率 |
| B、改变温度对反应速率无影响 |
| C、升高温度能加快反应速率 |
| D、使用催化剂能加快反应速率 |
 氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如图.下列有关氢氧燃料电池的说法不正确的是( )
氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如图.下列有关氢氧燃料电池的说法不正确的是( )| A、A电极是负极 |
| B、外电路中电子由B电极通过导线流向A电极 |
| C、产物为无污染的水,属于环境友好电池 |
| D、该电池的总反应:2H2+O2═2H2O |
在反应:H2+CuO
H2O+Cu中,H2作( )
| ||
| A、还原剂 | B、氧化剂 |
| C、还原产物 | D、氧化产物 |
下列物质是电解质的是( )
| A、Fe |
| B、SO3 |
| C、K2SO4 |
| D、C12H22O11(蔗糖) |
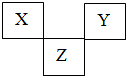 X、Y、Z是VA→VIIA族的三种短周期元素,他们在周期表中的位置如图所示.
X、Y、Z是VA→VIIA族的三种短周期元素,他们在周期表中的位置如图所示.