题目内容
1.某校化学学习小组拟验证NO能被氨气还原并测定其转化率,设计如下实验:参考知识:NO气体与FeSO4溶液反应生成可溶性硫酸亚硝基合铁(+2价):NO+FeSO4═Fe(NO)SO4
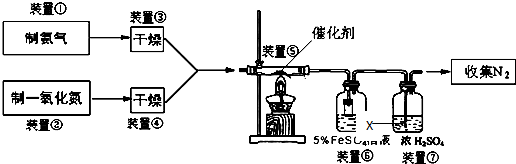
试回答下列问题:
(1)实验室常用氯化铵与氢氧化钙固体制备氨气,应选用的装置是A(填编号),该反应的化学方程式Ca(OH)2+2NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O.实验室制氨气还可用下图中装置BC(填编号).

(2)装置③、④若用同一装置,则该装置中所盛装的药品可以是D(填编号).
A.氯化钙 B.浓硫酸 C.五氧化二磷D.碱石灰
(3)装置⑥中,粗玻璃管X的作用防止倒吸,装置⑦的作用除去未反应的氨气并干燥N2.
(4)装置⑥的广口瓶中,除生成Fe(NO)SO4外,还有白色沉淀生成,写出生成该沉淀的离子方程式Fe2++2NH3+2H2O=Fe(OH)2↓+2NH4+.
(5)当进入装置⑤的NO为2.688L(标准状况,下同),氨气过量,最后收集到2.016LN2,则NO的转化率为90%.
分析 (1)根据实验室制氨气可以选用加热氯化铵与氢氧化钙固体的固固加热型或加热浓氨水的加热液体型或者向氧化钙等固体中滴加浓氨水的固液不加热型,据此分析;
(2)装置③干燥氨气选择和氨气不反应、不能溶解氨气的干燥剂;装置④是干燥一氧化氮气体,干燥剂不选强氧化性物质;
(3)装置⑥中,粗玻璃管X的作用防止倒吸,装置⑦是用来除去未反应的氨气,及其干燥N2;
(4)根据二价铁与氨水发生反应生成氢氧化亚铁沉淀书写;
(5)依据6NO+4NH3=5N2+6H2O的化学方程式计算反应的一氧化氮,结合转化率概念分析计算得到.
解答 解:(1)加热氯化铵与氢氧化钙固体制氨气为固固加热型,所以选A,方程式为:Ca(OH)2+2NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O,实验室制氨气还可用加热浓氨水的加热液体型或者向氧化钙等固体中滴加浓氨水的固液不加热型,所以可用选BC,故答案为:A;Ca(OH)2+2NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O; BC;
(2)装置③干燥氨气选择和氨气不反应、不能溶解氨气的干燥剂,装置④是干燥一氧化氮气体,干燥剂不选强氧化性物质,所以装置③、④若用同一装置,应选用碱性无强氧化性的物质即碱石灰,故选:D;
(3)装置⑥中,小段玻璃管的作用是防止氨气易溶于水发生倒吸现象;装置⑦是用来除去未反应的氨气,并且干燥氮气;
故答案为:防止倒吸;除去未反应的氨气并干燥N2;
(4)因为二价铁与氨水发生反应生成氢氧化亚铁沉淀,方程式为:Fe2++2NH3+2H2O=Fe(OH)2↓+2NH4+,故答案为:Fe2++2NH3+2H2O=Fe(OH)2↓+2NH4+;
(5)若进入装置⑤的NO共2688mL(已折算为标准状况,下同)物质的量=$\frac{2.688L}{22.4L/mol}$=0.12mol,氨气过量,最后收集到标准状况下2016mL N2,物质的量=$\frac{2.016L}{22.4L/mol}$=0.09mol;6NO+4NH3=5N2+6H2O,依据反应化学方程式计算反应的一氧化氮物质的量=$\frac{6×0.09mol}{5}$=0.108mol,则NO的转化率=$\frac{0.108mol}{0.12mol}$×100%=90%;
故答案为:90%.
点评 本题考查了物质现在的实验验证和反应现象的判断应用,化学方程式的计算应用,掌握基础是解题关键,题目难度中等.

| A. | c(H+) | B. | c(HCO${\;}_{3}^{-}$) | ||
| C. | c(H+)•c(OH-) | D. | $\frac{c(O{H}^{-})•c(HC{{O}_{3}}^{-})}{c(C{{O}_{3}}^{2-})}$ |
| A. | 金属钠投入水中的离子方程式;Na+2H2O=Na++2OH-+O2↑ | |
| B. | 常温下,0.1mol/L氯化铵溶液pH=5的原因:NH4++H2O?NH3•H2O+H+ | |
| C. | 用惰性电极电解饱和食盐水的阳极反应式:2Cl--2e-=Cl2↑ | |
| D. | 乙醛与新制的氢氧化铜悬浊液反应的离子方程式:CH3CHO+2Cu(OH)2+OH-$\stackrel{△}{→}$CH3COO-+Cu2O↓+3H2O |
| A. | Y,Z形成的分子空间构型可能是正四面体 | |
| B. | W,Y,Z的电负性大小顺序一定是Z>Y>W | |
| C. | WY2分子中δ键与π键的数目之比是2:1 | |
| D. | W,X,Y,Z的原子半径大小顺序可能是W>X>Y>Z |
| A. | 2900kJ | B. | 2680kJ | C. | 3120kJ | D. | 2856kJ |
| A. | 氯化铁溶液中滴入KSCN后溶液变为血红色 | |
| B. | 将钠投入水中所得溶液中含有Na+,OH-和H2O分子 | |
| C. | 氯气溶解于水得到的氯水中既含有Cl2,H2O分子,又含有H+,Cl2,HClO等微粒 | |
| D. | 向硝酸银溶液中加入少量的铜粉,充分反应后往上层清夜中滴加KBr溶液呈浅黄色 |
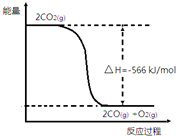 已知:①2CO(g)+O2(g)═2CO2(g)△H=-566kJ•mol-1
已知:①2CO(g)+O2(g)═2CO2(g)△H=-566kJ•mol-1②Na2O2(s)+CO2(g)═Na2CO3(s)+$\frac{1}{2}$O2(g)△H=-226kJ•mol-1
( )
| A. | CO的燃烧热为566kJ•mol-1 | |
| B. | 如图可表示①反应过程中的能量变化 | |
| C. | Na2O2(s)+CO(g)═Na2CO3(s)△H=-509kJ•mol-1 | |
| D. | 由②可知,反应生成Na2CO3固体106g,放出热量226kJ•mol-1 |