题目内容
ClO2是一种杀菌消毒效率高、二次污染小的水处理剂.下列反应可制得ClO2:2KClO3+H2C2O4+H2SO4
2ClO2↑+K2SO4+2CO2↑+2H2O.下列判断正确的是( )
| ||
| A、KClO3在反应中失去电子 |
| B、H2C2O4是氧化剂 |
| C、H2SO4发生氧化反应 |
| D、生成2mol ClO2时有2mol电子转移 |
考点:氧化还原反应
专题:氧化还原反应专题
分析:该反应中Cl元素化合价由+5价变为+4价,C元素化合价由+3价变为+4价,
A.元素失电子化合价升高;
B.得电子化合价降低的反应物是氧化剂;
C.还原剂发生氧化反应;
D.根据二氧化氯和转移电子之间的关系式计算.
A.元素失电子化合价升高;
B.得电子化合价降低的反应物是氧化剂;
C.还原剂发生氧化反应;
D.根据二氧化氯和转移电子之间的关系式计算.
解答:
解:该反应中Cl元素化合价由+5价变为+4价,C元素化合价由+3价变为+4价,
A.该反应中Cl元素化合价由+5价变为+4价,所以KClO3在反应中得到电子,故A错误;
B.C元素化合价由+3价变为+4价,所以草酸失电子化合价升高,则草酸作还原剂,故B错误;
C.硫酸中各元素化合价不变,所以硫酸既不发生氧化反应也不发生还原反应,故C错误;
D.生成2mol ClO2时转移电子的物质的量=2mol×(5-4)=2mol,故D正确;
故选D.
A.该反应中Cl元素化合价由+5价变为+4价,所以KClO3在反应中得到电子,故A错误;
B.C元素化合价由+3价变为+4价,所以草酸失电子化合价升高,则草酸作还原剂,故B错误;
C.硫酸中各元素化合价不变,所以硫酸既不发生氧化反应也不发生还原反应,故C错误;
D.生成2mol ClO2时转移电子的物质的量=2mol×(5-4)=2mol,故D正确;
故选D.
点评:本题考查了氧化还原反应,根据元素化合价变化结合基本概念来分析解答,熟悉元素的化合价是解本题关键,知道转移电子的计算方法,难度不大.

练习册系列答案
相关题目
下列说法正确的是( )
| A、乙酸的分子式:C2H4O |
| B、甲烷的分子式:CH4 |
| C、乙酸的结构简式:CH3CH2OH |
| D、乙烷的结构简式:C2H6 |
用NA表示阿佛加德罗常数,下列说法正确的是( )
| A、22.4L O2的物质的量约为1mol |
| B、标准状况下,11.2L H2O的物质的量约为0.5mol |
| C、1 L 1mol/L的NaOH溶液中Na+的物质的量为1 mol |
| D、5.6gmol铁与足量的盐酸完全反应,铁失去的电子数为0.1NA |
工业上利用反应:3C12+2NH3=N2+6HCl检查氯气管道是否漏气.下列说法错误的是( )
| A、该反应中C12是氧化剂 |
| B、若管道漏气遇氨会产生白烟 |
| C、该反应生成1 mol N2,有6 mol电子发生转移 |
| D、该反应中氨气发生还原反应 |
如图是某有机物分子的球棍模型.关于该物质的说法正确的是( )
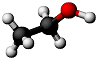

| A、可以与醋酸发生中和反应 |
| B、能与钠发生取代反应 |
| C、能使紫色石蕊试液变红色 |
| D、能发生催化氧化反应 |
日本地震引起放射性13153I原子发生泄漏,该原子对环境会造成污染.下列关于这种原子的说法正确的是( )
| A、电子数是78 |
| B、中子数是131 |
| C、质量数是53 |
| D、质子数是53 |