题目内容
8.工业上用58吨丁烷氧化法制醋酸.反应的化学方程式可表示为:2C4H10+5O2$\stackrel{一定条件}{→}$4CH3COOH+2H2O(1)需要标准状况下的空气2.8×105m3(空气中O2、N2的体积分数分别为0.2、0.8)
(2)若生成的醋酸全部溶解在生成的水中,所得醋酸的质量分数为86.96%(保留两位有效数字).
分析 (1)令O2需要的物质的量为xmol,根据方程式中计算氧气的物质的量,结合氧气在空气中的含量计算需要空气的体积;
(2)令生成水y吨,根据方程式计算生成水的质量;令生成醋酸m吨,根据方程式计算生成醋酸的质量,根据质量分数的定义计算.
解答 解:(1)令O2需要的物质的量为xmol,则:
2 C4H10+5O2$\stackrel{一定条件}{→}$4CH3COOH+2H2O,
58×2g 5mol
58×106 xmol
所以x=$\frac{5×58×1{0}^{6}}{2×58}$=2.5×106
所以需要空气的体积为$\frac{2.5×1{0}^{{6}^{\;}}mol×22.4L/mol}{0.2}$=2.8×108L=2.8×105m3,故答案为:2.8×105;
(2)令生成水y吨,则:
2 C4H10+5 O2$\stackrel{一定条件}{→}$4CH3COOH+2H2O,
58×2g 18×2g
58吨 y吨
所以y=$\frac{58×2×18}{58×2}$=18,
令生成醋酸m吨,则:
2 C4H10+5 O2$\stackrel{一定条件}{→}$4CH3COOH+2H2O,
58×2g 4×60g
58吨 m吨
所以m=$\frac{58×4×60}{58×2}$=120
生成的醋酸溶解在生成的水中,所得醋酸的质量分数为$\frac{120t}{120t+18t}$×100%=86.96%.
故答案为:86.96.
点评 本题考查根据方程式的计算,难度中等,计算量较大,需细心计算,旨在考查学生对数据处理及利用方程式进行计算.

| A. | 乙烯的结构式:C2H4 | B. | 甲烷分子的比例模型: | ||
| C. | 四氯化碳的电子式: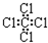 | D. | 苯的分子式: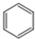 |
| A. | Ca2+ | B. | Mg2+ | C. | Na+ | D. | H+ |
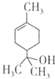
| A. | 1mol该物质最多能和lmol氢气发生加成反应 | |
| B. | 该物质属于烃的衍生物 | |
| C. | 该物质能使溴水褪色 | |
| D. | 分子式为C10H20O |
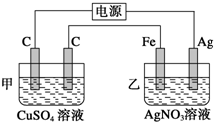 用如图所示的装置进行电解,在通电一段时间后,铁电极的质量增加.
用如图所示的装置进行电解,在通电一段时间后,铁电极的质量增加.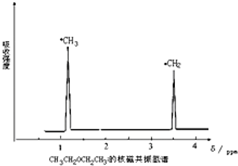 利用核磁共振技术测定有机物分子的三维结构的研究获得了2002年诺贝尔化学奖.在有机物分子中,不同氢原子的核磁共振谱中给出的峰值(信号)也不同,根据峰值(信号)可以确定有机物分子中氢原子的种类和数目.例如二乙醚的结构简式为:CH3-CH2-O-CH2-CH3,其核磁共振谱中给出的峰值(信号)有两个,如图所示:
利用核磁共振技术测定有机物分子的三维结构的研究获得了2002年诺贝尔化学奖.在有机物分子中,不同氢原子的核磁共振谱中给出的峰值(信号)也不同,根据峰值(信号)可以确定有机物分子中氢原子的种类和数目.例如二乙醚的结构简式为:CH3-CH2-O-CH2-CH3,其核磁共振谱中给出的峰值(信号)有两个,如图所示: