题目内容
19. 对硫一氮化合物的研究是最为活跃的领域之一.如图是已经合成典型的硫-氮化合物的分子结构.下列说法正确的是( )
对硫一氮化合物的研究是最为活跃的领域之一.如图是已经合成典型的硫-氮化合物的分子结构.下列说法正确的是( )| A. | 该物质的分子式为SN | B. | 该物质具有很高的熔、沸点 | ||
| C. | 该分子是非平面的八元环结构 | D. | 该物质与S2N2互为同素异形体 |
分析 A.该物质的分子式为S4N4;
B.分子晶体的熔沸点一般较低;
C.根据分子的结构图判断;
D.由同种元素组成的不同单质互称同素异形体,同素异形体首先必须是单质.
解答 解:A.由图知该物质的分子中含有4个S和4个N,则该物质的分子式为S4N4,故A错误;
B.该物质存在分子,属于分子晶体,分子晶体的熔沸点一般较低,故B错误;
C.由图知该物质的分子中含有4个S和4个N,由8个原子构成的8元环,8个原子不在同一平面,故C正确;
D.由同种元素组成的不同单质互称同素异形体,S2N2和S4N4都是化合物,故D错误.
故选C.
点评 本题考查分子构型的判断、分子结构、同素异形体,题目难度不大,注意分子晶体的熔沸点一般较低,侧重于考查学生的分析能力和应用能力.

练习册系列答案
 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案
相关题目
9.目前全球掀起新一轮探月高潮.月球上蕴藏着丰富的氦-3(3He),用它可以给核聚变提供能源.关于3He的下列说法中正确的是( )
| A. | 3He与3H中含有相同的中子数 | |
| B. | 通过化学反应可以实现3He与4He的相互转化 | |
| C. | 1 mol氦气含有质子数为2 mol | |
| D. | 3He与4He互为同素异形体 |
10.一定温度下,将 2mol SO2 和 1mol O2充入一定容密闭容器中,在催化剂存在下进行下列反应:2SO2(g)+O2(g)?2SO3(g);△H=-197kJ/mol,下列说法中正确的是( )
| A. | 达到反应限度时,生成 SO3 为2 mol | |
| B. | 达到反应限度时,反应放出 197 kJ 的热量 | |
| C. | 达到反应限度时SO2、O2、SO3的分子数之比一定为2:1:2 | |
| D. | 达到反应限度时SO2的消耗速率必定等于SO3的消耗速率 |
7.对于有机物 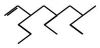 命名正确的是( )
命名正确的是( )
 命名正确的是( )
命名正确的是( )| A. | 5,7-二甲基-3-乙基-1-辛烯 | B. | 3-乙基-5,7-二甲基-1-壬烯 | ||
| C. | 3-甲基-5-乙基-7-丙基-8-壬烯 | D. | 7-甲基-5-乙基-3-丙基-1-壬烯 |
14.X、Y、Z、W、R是5种短周期元素,其原子序数依次增大.X是周期表中原子半径最小的元素,Y原子最外层电子数是次外层电子数的3倍,Z、W、R处于同一周期,R与Y处于同一族,Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相等.下列说法正确的是 ( )
| A. | 元素Y、Z、W具有相同电子层结构的离子,其半径依次增大 | |
| B. | 元素X与元素Y形成的化合物X2Y2中既有极性共价键又有非极性共价键 | |
| C. | 元素Y、R分别与元素X形成的化合物的热稳定性:XmY<XmR | |
| D. | 元素W、R的最高价氧化物的水化物都是强酸 |
4.某有机物的分子式为C5H10O,它能发生银镜反应和加成反应,若将它与H2加成,所得产物结构简式可能是( )
| A. | (CH3)3CCH2OH | B. | (CH3CH2)2CHOH | C. | CH3(CH2)2CH(CH3)OH | D. | CH3CH2C(CH3)2OH |
11.下列物质属于离子化合物的是( )
| A. | H2O | B. | HCl | C. | NaCl | D. | CO2 |
9. 298K时,分别向体积、浓度均为20mL0.1mol•L-1的HX溶液、HY溶液中滴加等浓度的NaOH 溶液,混合溶液的pH与加入NaOH溶液体积(V)之间的关系如图所示.(注明:弱电解质的电离度等于已电离的电解质的量与电解质总量之比)下列说法正确的是( )
298K时,分别向体积、浓度均为20mL0.1mol•L-1的HX溶液、HY溶液中滴加等浓度的NaOH 溶液,混合溶液的pH与加入NaOH溶液体积(V)之间的关系如图所示.(注明:弱电解质的电离度等于已电离的电解质的量与电解质总量之比)下列说法正确的是( )
 298K时,分别向体积、浓度均为20mL0.1mol•L-1的HX溶液、HY溶液中滴加等浓度的NaOH 溶液,混合溶液的pH与加入NaOH溶液体积(V)之间的关系如图所示.(注明:弱电解质的电离度等于已电离的电解质的量与电解质总量之比)下列说法正确的是( )
298K时,分别向体积、浓度均为20mL0.1mol•L-1的HX溶液、HY溶液中滴加等浓度的NaOH 溶液,混合溶液的pH与加入NaOH溶液体积(V)之间的关系如图所示.(注明:弱电解质的电离度等于已电离的电解质的量与电解质总量之比)下列说法正确的是( )| A. | 298K 时,0.1mol•L-1HX 溶液中HX的电离度为1% | |
| B. | V=10mL时,同时微热溶液(忽略体积变化),$\frac{c({X}^{-})}{c({Y}^{-})}$逐渐增大 | |
| C. | V=20mL 时,HX曲线对应的溶液中c(Na+)=c(X-)>c(H+)=c(OH-) | |
| D. | 滴定这两种溶液时都可以选择甲基橙替代酚酞作指示剂 |