题目内容
6.由丙烯经下列反应可制得F、G两种高分子化合物,它们都是常用的塑料.
①丙烯分子中,最多有7个原子在同一个平面上;
②聚合物F的结构简式是
 ;
;③B转化为C的化学方程式是
 ;C与银氨溶液反应的化学方程式为
;C与银氨溶液反应的化学方程式为 .
.
分析 CH3CH=CH2与溴发生加成反应生成A为CH3CHBrCH2Br,在碱性条件下水解生成B为CH3CHOHCH2OH,进而被催化氧化为C,即 ,进一步被氧化为D,D生成E的反应是原子利用率100%的反应且D不能使溴的四氯化碳溶液褪色,即D为
,进一步被氧化为D,D生成E的反应是原子利用率100%的反应且D不能使溴的四氯化碳溶液褪色,即D为 ,D发生加成反应生成E,则E为CH3CH(OH)COOH,CH3CH=CH2可发生加聚反应生成高聚物,F为
,D发生加成反应生成E,则E为CH3CH(OH)COOH,CH3CH=CH2可发生加聚反应生成高聚物,F为 ,以此来解答.
,以此来解答.
解答 解:①丙烯分子中,碳碳双键为平面结构,甲基为四面体结构,则甲基中有2个H与其它原子不共面,最多有7个原子在同一个平面上,故答案为:7;
②聚合物F的结构简式是 ,故答案为:
,故答案为: ;
;
③B为CH3CHOHCH2OH,在催化剂条件下被氧化生成C为 ,反应的方程式为
,反应的方程式为 ,
,
C中含有醛基能发生银镜反应,则C与银氨溶液的反应为 ,
,
故答案为: ;
; .
.
点评 本题考查有机物的推断及有机物的结构和性质,为高频考点,综合性较强,注意利用反应条件及物质的官能团来分析是解答本题的关键,侧重分析与应用能力的考查,题目难度中等.

练习册系列答案
相关题目
12.W、X、Y、Z为四种短周期元素,且原子序数依次增大.W的一种核素可用于测定文物的年代,X的一种同素异形体具有漂白性且可用于自来水消毒,Y单质在X单质中燃烧生成淡黄色固体,Z的简单离子半径是同周期元素简单离子半径最小的.下列说法正确的是( )
| A. | X与Y可形成两种阴阳离子个数比相同的化合物 | |
| B. | W与X的单质可直接化合形成含有非极性键的化合物 | |
| C. | Z单质制造的容器可长时间储存碱性的食物 | |
| D. | 工业上常采用电解熔融Z的氯化物来制取单质Z |
1.下列物质都能与足量的KI溶液(含少量硫酸)反应生成I2,当生成等量的I2时,消耗物质的量最小的是( )
| A. | H2O2 | B. | FeCl3 | C. | KMnO4 | D. | KIO3 |
11.用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 1molNa分别与足量的O2反应生成N2O或Na2O2,失去的电子数均为NA | |
| B. | 通常状况下,39g Na2O2固体中含有的离子总数为2 Na2O2 | |
| C. | 标准状况下,11gCO2含有的共用电子对数为0.5 NA | |
| D. | 滴加沸水中的FeC13溶液有5.6gFe3+发生水解,则生成的胶粒数为0.1NA |
18. 已知A是一种常见的非金属单质,B是氧化物,E是A的氢化物,D是A的最高价氧化物对应的水化物,上述物质间的转化关系如图所示.下列说法错误的是( )
已知A是一种常见的非金属单质,B是氧化物,E是A的氢化物,D是A的最高价氧化物对应的水化物,上述物质间的转化关系如图所示.下列说法错误的是( )
 已知A是一种常见的非金属单质,B是氧化物,E是A的氢化物,D是A的最高价氧化物对应的水化物,上述物质间的转化关系如图所示.下列说法错误的是( )
已知A是一种常见的非金属单质,B是氧化物,E是A的氢化物,D是A的最高价氧化物对应的水化物,上述物质间的转化关系如图所示.下列说法错误的是( )| A. | 若E、D的水溶液均呈酸性,则A为硫 | |
| B. | 若D是一种难溶于水的物质,则A为硅 | |
| C. | 若E、D的水溶液均呈酸性,则B能与水反应 | |
| D. | 若D是一种难溶于水的物质,则B能与水反应 |
15.下列说法中正确的是( )
| A. | 溶液中的溶质粒子能透过滤纸,而胶体中的分散质粒子不能透过滤纸,所以可以用滤纸来分离溶液和胶体 | |
| B. | 有化学键断裂或化学键形成的过程都是化学变化 | |
| C. | 焰色反应属于吸热反应 | |
| D. | 食盐溶液能导电,但食盐溶液不是电解质 |
14.下列化学用语的书写,正确的是( )
| A. | 水分子的结构式: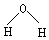 | B. | 氯原子的结构示意图: | ||
| C. | 溴化钠的电子式: | D. | 氮气的电子式: |


