题目内容
5.对于下列事实的解释错误的是( )| A. | 在蔗糖中加入浓硫酸后出现发黑现象,说明浓硫酸具有脱水性 | |
| B. | 浓硝酸在光照下颜色变黄,说明浓硝酸不稳定 | |
| C. | 常温下,浓硝酸可以用铝罐贮存,说明铝与浓硝酸不反应 | |
| D. | 氨水可使酚酞试剂变为红色,说明氨溶解于水显弱碱性 |
分析 A.浓硫酸具有脱水性,可使蔗糖碳化;
B.硝酸见光分解;
C.铝与浓硝酸发生钝化反应;
D.氨气和水反应生成一水合氨,为弱碱.
解答 解:A.浓硫酸具有脱水性,可使蔗糖脱水而碳化,故A正确;
B.硝酸见光分解,生成的二氧化氮溶液硝酸而使硝酸变黄,故B正确;
C.铝与浓硝酸发生钝化反应,在表面生成一层致密的氧化膜,可用铝罐贮存硝酸,故C错误;
D.氨气和水反应生成一水合氨,可电离生成氢氧根离子,为弱碱,故D正确.
故选C.
点评 本题综合考查元素化合物知识,为高频考点,侧重于学生分析能力以及元素化合物知识的综合理解和运用的考查,注意相关基础知识的积累,难度不大.

练习册系列答案
相关题目
13.下列有关原子结构和元素周期律表述正确的是( )
| A. | 原子序数为15的元素的最高化合价为+3 | |
| B. | ⅦA族元素是同周期中非金属性最强的元素 | |
| C. | 原子序数为12的元素位于元素周期表的第三周期ⅡA族 | |
| D. | 第二周期ⅣA族元素的原子核电荷数和中子数一定为6 |
20.下列图示与对应的叙述不相符的是( )
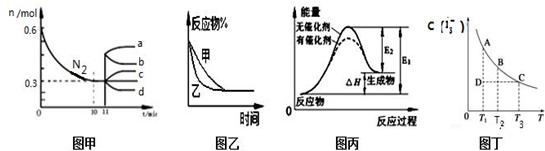

| A. | 图甲表示在 2L 的密闭容器中发生合成氨反应时 N2 的物质的量随时间的变化曲线,从 11min 起其它条件不变,压缩容器的体积为 1L,则 n(N2)的变化曲线为 d | |
| B. | 图乙表示压强对可逆反应 2A(g)+2B(g)?3C(g)+D(g)的影响,乙的压强比甲的压强大 | |
| C. | 图丙表示的反应是吸热反应,该图表明催化剂不能改变化学反应的焓变 | |
| D. | 图丁表示反应:I2(aq)+I-(aq)?I-3(aq)进行到状态 D 时一定有v 逆>v 正 |
10.下列分子中的中心原子杂化轨道的类型相同的是( )
| A. | SO3与SO2 | B. | BF3与NH3 | C. | BeCl2与SO2 | D. | H2O与SCl2 |
17.下列说法正确的是( )
| A. | 所有不锈钢都只含有金属元素 | |
| B. | 大多数金属元素均以单质形式存在于自然界 | |
| C. | 广东正在打捞的明代沉船上存在大量铝制餐具 | |
| D. | 镁合金的硬度和强度均高于纯镁 |
14.二甲醚和乙醇是同分异构体,其鉴别可采用化学方法及物理方法,下列鉴别方法中不能对二者进行鉴别的是( )
| A. | 利用铜丝燃烧法 | B. | 利用质谱法 | ||
| C. | 利用红外光谱法 | D. | 利用核磁共振氢谱 |

 .
. ClO2是一种国际上公认的安全无毒的绿色水处理剂.回答下列问题:
ClO2是一种国际上公认的安全无毒的绿色水处理剂.回答下列问题: