题目内容
下列分离、提纯、物质的检验方法错误的是( )
| A、硝酸钠中含有少量的氯化钠:加水配成热饱和溶液,然后冷却结晶后过滤得到硝酸钠晶体 |
| B、氧化钙固体中混有的少量的碳酸钙,用加热分解法方法除去碳酸钙 |
| C、焰色反应实验中铂丝蘸取待测物之前先用稀硫酸洗净 |
| D、配置一定物质的量浓度溶液时,容量瓶中液面离标线1-2cm处时改用胶头滴管定容 |
考点:物质的分离、提纯和除杂,物质的检验和鉴别的基本方法选择及应用
专题:实验评价题
分析:A.硝酸钾的溶解度随温度升高而升高,氯化钠的溶解度受温度变化影响不大;
B.碳酸钙在高温下分解生成氧化钙和二氧化碳;
C.根据硫酸盐难挥发,氯化物易挥发来解答;
D.容量瓶中液面离标线1-2cm处时改用胶头滴管定容.
B.碳酸钙在高温下分解生成氧化钙和二氧化碳;
C.根据硫酸盐难挥发,氯化物易挥发来解答;
D.容量瓶中液面离标线1-2cm处时改用胶头滴管定容.
解答:
解:A.不同物质的溶解度受温度变化影响不同,硝酸钾的溶解度随温度升高而升高,氯化钠的溶解度受温度变化影响不大.将含有少量氯化钠杂质的硝酸钾热饱和溶液,冷却析出晶体后,剩余的溶液仍为硝酸钾的饱和溶液,故A正确;
B.碳酸钙在高温下分解生成氧化钙和二氧化碳,能除去杂质且没有引入新的杂质,符合除杂原则,故B正确;
C.因金属丝在使用前要用稀盐酸将其表面的氧化膜洗净,然后在火焰上灼烧至无焰色.不能选用稀硫酸来洗涤,因为生成的硫酸盐沸点很高,不易除去而干扰火焰的颜色.而金属氧化物跟稀盐酸反应生成的氯化物灼烧时易汽化而挥发不影响火焰的颜色,故C错误;
D.配制溶液时,容量瓶中液面离标线1-2cm处时改用胶头滴管定容,故D正确.
故选C.
B.碳酸钙在高温下分解生成氧化钙和二氧化碳,能除去杂质且没有引入新的杂质,符合除杂原则,故B正确;
C.因金属丝在使用前要用稀盐酸将其表面的氧化膜洗净,然后在火焰上灼烧至无焰色.不能选用稀硫酸来洗涤,因为生成的硫酸盐沸点很高,不易除去而干扰火焰的颜色.而金属氧化物跟稀盐酸反应生成的氯化物灼烧时易汽化而挥发不影响火焰的颜色,故C错误;
D.配制溶液时,容量瓶中液面离标线1-2cm处时改用胶头滴管定容,故D正确.
故选C.
点评:本题考查物质的分离和提纯、焰色反应和溶液配制,题目难度不大,本题注意相关物质的性质的异同,为解答该题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列说法不正确的是( )
| A、除去乙酸乙酯中残留的乙酸,可加过量饱和Na2CO3溶液振荡后,静置分液 |
| B、某烷烃主链4个碳原子数的同分异构体有2种,则与其碳原子个数相同的且主链4个碳原子的单烯烃有4种 |
C、1mol有机物 与NaOH溶液反应,最多消耗5mol NaOH 与NaOH溶液反应,最多消耗5mol NaOH |
D、有机物 分子中所有原子在同一平面内 分子中所有原子在同一平面内 |
向含Al2(SO4)3和AlCl3的混合溶液中逐滴加入1mol/L Ba(OH)2溶液至过量,加入Ba(OH)2溶液的体积和所得沉淀的物质的量的关系如图,下列说法不正确的是( )
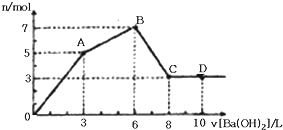

| A、OA段反应的离子方程式为:3Ba2++2Al3++8OH-+3SO42-═3BaSO4↓+2AlO2-+4H2O |
| B、向D点溶液中通入C02气体,立即产生白色沉淀 |
| C、原混合液中c[Al2(SO4)3]:c(AlCl3)═1:2 |
| D、图中C点铝元素存在形式是AlO2- |
氢化钙可作为生氢剂,化学方程式是CaH2+2H2O═Ca(OH)2+2H2↑,下列有关叙述正确的是( )
| A、氢化钙被还原 |
| B、水既是氧化剂,又是还原剂 |
| C、H2既是氧化产物,也是还原产物 |
| D、H2O发生氧化反应 |
下列各组顺序的排列不正确的是( )
| A、离子半径:F->Na+>Mg2+>Al3+ |
| B、热稳定性:HCl>H2S>PH3>AsH3 |
| C、酸性强弱:H3AlO3<H4SiO4<H2CO3<H3PO4 |
| D、沸点:HF<HCl<HBr<HI |
下列说法中正确的是( )
| A、.将NaHSO4晶体加热熔融时有两种化学键断裂 |
| B、水分子间因为存在氢键,所以加热至较高温度时也难以分解 |
| C、根据金属晶体的共性可知金属键和离子键一样没有方向性和饱和性 |
| D、以极性共价键形成的分子一定是极性分子 |
下列物质中属于电解质的是( )
| A、蔗糖 |
| B、CO2 |
| C、CaCO3 |
| D、Al |
下列排列顺序不正确的是( )
| A、热稳定性:HF>HCl>HBr |
| B、原子半径:Na>S>O |
| C、离子半径:Mg2+>O2->F- |
| D、酸性:HClO4>H2SO4>H3PO4 |

