题目内容
14.按要求书写相应结构或名称(1)2,6-二甲基-4-乙基辛烷CH3CH(CH3)CH2CH(CH2CH3)CH2CH(CH3)CH2CH3
(2)2-甲基-1-戊烯CH2=CH(CH3)CH2CH2CH3
(3)有机物 CH3CH2COOH 的名称丙酸
(4)有机物
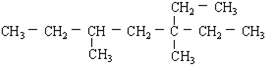 的名称3,5-二甲基-3-乙基庚烷
的名称3,5-二甲基-3-乙基庚烷(5)
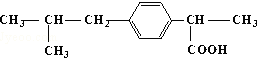 所含官能团的名称羧基
所含官能团的名称羧基(6)
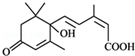 所含官能团的名称碳碳双键、羟基、羰基、羧基.
所含官能团的名称碳碳双键、羟基、羰基、羧基.
分析 (1)最长的主链含有8个C原子,甲基处于2、6号碳原子上,乙基处于4号碳原子上,据此书写;
(2)含有C=C双键的碳链有5个碳原子,双键处于端位置,从C=C双键一端编号,甲基处于2号碳原子上;
(3)含有羧基,名称为酸;
(4)碳链最长称某烷,靠近支链把号编.简单在前同相并,其间应划一短线;
(5)苯环不是官能团;
(6)含有碳碳双键、羟基、羰基、羧基.
解答 解:(1)2,6-二甲基-4-乙基辛烷中最长的主链含有8个C原子,甲基处于2、6号碳原子上,乙基处于4号碳原子上,其结构简式为CH3CH(CH3)CH2CH(CH2CH3)CH2CH(CH3)CH2CH3,
故答案为:CH3CH(CH3)CH2CH(CH2CH3)CH2CH(CH3)CH2CH3;
(2)2-甲基-1-戊烯分子中含有C=C双键的碳链有5个碳原子,双键处于端位置,从C=C双键一端编号,甲基处于2号碳原子上,其结构简式为CH2=CH(CH3)CH2CH2CH3,
故答案为:CH2=CH(CH3)CH2CH2CH3;
(3)CH3CH2COOH 的名称丙酸,故答案为:丙酸;
(4)最长的碳链为7个碳原子,名称为3,5-二甲基-3-乙基庚烷,故答案为:3,5-二甲基-3-乙基庚烷;
(5) 官能团为羧基,故答案为:羧基;
官能团为羧基,故答案为:羧基;
(6) 所含官能团为碳碳双键、羟基、羰基、羧基,故答案为:碳碳双键、羟基、羰基、羧基.
所含官能团为碳碳双键、羟基、羰基、羧基,故答案为:碳碳双键、羟基、羰基、羧基.
点评 本题考查有机物的命名、有机物结构、官能团等,难度中等,注意掌握有机物的命名原则,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
17.一种以NaBH4和H2O2为原料的新型电池的工作原理如图所示.下列说法错误的是( )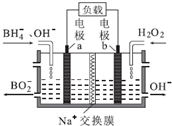

| A. | 电池的正极反应为H2O2+2e-=2OH- | |
| B. | 电池放电时Na+从a极区移向b极区 | |
| C. | 电子从电极b经外电路流向电极a | |
| D. | b极室的输出液经处理后可输入a极室循环利用 |
5.等质量的下列物质燃烧,消耗氧气量最多的是( )
| A. | CH4 | B. | C2H6 | C. | C3H6 | D. | C3H8 |
2.在氧、氟、钠、氯四种元素中,原子半径最大的元素是( )
| A. | 氧 | B. | 氟 | C. | 钠 | D. | 氯 |
19.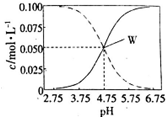 室温条件下在醋酸、醋酸钠混合溶液中,当c(CH3COOH)+c(CH3COO-)=0.lmol.L-1时,c(CH3COOH)、c(CH3COO-)与pH的关系如图所示.下列有关叙述正确的是( )
室温条件下在醋酸、醋酸钠混合溶液中,当c(CH3COOH)+c(CH3COO-)=0.lmol.L-1时,c(CH3COOH)、c(CH3COO-)与pH的关系如图所示.下列有关叙述正确的是( )
 室温条件下在醋酸、醋酸钠混合溶液中,当c(CH3COOH)+c(CH3COO-)=0.lmol.L-1时,c(CH3COOH)、c(CH3COO-)与pH的关系如图所示.下列有关叙述正确的是( )
室温条件下在醋酸、醋酸钠混合溶液中,当c(CH3COOH)+c(CH3COO-)=0.lmol.L-1时,c(CH3COOH)、c(CH3COO-)与pH的关系如图所示.下列有关叙述正确的是( )| A. | pH=5.5的溶液中:c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-) | |
| B. | 向W点所表示的1.0L溶液中通人0.05molHCl气体(溶液体积变化可忽略):c(H+)=c(CH3COOH)+c(OH-) | |
| C. | W点所表示的溶液中:c(Na+)+c(H+)=c(CH3COOH)+c(OH)- | |
| D. | pH=3.5的溶液中:c(Na+)+c(H+)+c(OH-)+c(CH3COOH)=0.1mol.L-l |
6.直接排放含SO2,的烟气会形成胶雨,危害环境.利用钠碱循环法可脱除烟气中的SO2.
(1)用化学方程式表示SO2形成硫酸型酸雨的反应:SO2+H2O?H2SO3、2H2SO3+O2=2H2SO4.
(2)在钠碱循环法中,Na2SO3溶液作为吸收液,可由NaOH溶液吸收SO2制得,该反应的离子方程式是2OH-+SO2=SO32-+H2O.
(3)吸收液吸收SO2的过程中,pH随n(SO32-):n(HSO3-)变化关系如下表:
①上表判断NaHSO3溶液显酸性,用化学平衡原理解释:HSO3-存在HSO3-?H++SO32-和HSO3-+H2O?H2SO3+OH-,HSO3-的电离程度大于水解程度.
②当吸收液呈中性时,溶液中离子浓度关系正确的是ab
a.c(Na+)═2c(SO32-)+c(HSO3-)
b.c(Na+)>c(HSO3-)>c(SO32-)>c(H +)═c(OH-)
c.c(Na+)+c(H +)═c(SO32-)+c(HSO3-)+c(OH-)
(4)当吸收液的pH降至约为6时,送至电解槽再生.再生示意图如下:

①HSO3-在阳极放电的电极反应式是HSO3-+H2O-2e-=SO42-+3H+.
②当阴极室中溶液pH升至8以上时,吸收液再生并循环利用.简述再生原理:氢离子在阴极得电子生成氢气,溶液中氢离子浓度降低,促使HSO3-电离生成SO32-,且钠离子进入阴极室,吸收液就可以再生.
(1)用化学方程式表示SO2形成硫酸型酸雨的反应:SO2+H2O?H2SO3、2H2SO3+O2=2H2SO4.
(2)在钠碱循环法中,Na2SO3溶液作为吸收液,可由NaOH溶液吸收SO2制得,该反应的离子方程式是2OH-+SO2=SO32-+H2O.
(3)吸收液吸收SO2的过程中,pH随n(SO32-):n(HSO3-)变化关系如下表:
| n(SO32-):n(HSO3-) | 91:9 | 1:1 | 1:91 |
| pH | 8.2 | 7.2 | 6.2 |
②当吸收液呈中性时,溶液中离子浓度关系正确的是ab
a.c(Na+)═2c(SO32-)+c(HSO3-)
b.c(Na+)>c(HSO3-)>c(SO32-)>c(H +)═c(OH-)
c.c(Na+)+c(H +)═c(SO32-)+c(HSO3-)+c(OH-)
(4)当吸收液的pH降至约为6时,送至电解槽再生.再生示意图如下:

①HSO3-在阳极放电的电极反应式是HSO3-+H2O-2e-=SO42-+3H+.
②当阴极室中溶液pH升至8以上时,吸收液再生并循环利用.简述再生原理:氢离子在阴极得电子生成氢气,溶液中氢离子浓度降低,促使HSO3-电离生成SO32-,且钠离子进入阴极室,吸收液就可以再生.
3.1,2-二氯乙烯可以形成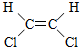 与
与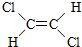 两种不同的空间异构体,下列物质中,能形成类似上述两种空间异构体的是( )
两种不同的空间异构体,下列物质中,能形成类似上述两种空间异构体的是( )
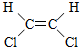 与
与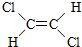 两种不同的空间异构体,下列物质中,能形成类似上述两种空间异构体的是( )
两种不同的空间异构体,下列物质中,能形成类似上述两种空间异构体的是( )| A. | 1,1-二氯乙烯 | B. | 丙烯 | C. | 2-丁烯 | D. | 1-丁烯 |
4.化学与生活、社会发展息息相关,下列有关说法正确的是( )
| A. | “青蒿一握,以水二升渍,绞取汁”,屠呦呦对青蒿素的提取属于化学变化 | |
| B. | “丹砂(HgS)烧之成水银,积变又还成了丹砂”,该过程发生了分解、化合、氧化还原反应 | |
| C. | 干燥剂硅胶和硅橡胶的主要化学成分都是二氧化硅 | |
| D. | 铜制品在潮湿的空气中生锈,其主要原因是发生了析氢腐蚀 |