题目内容
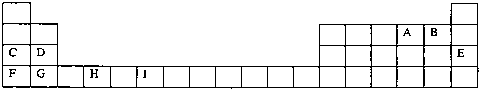
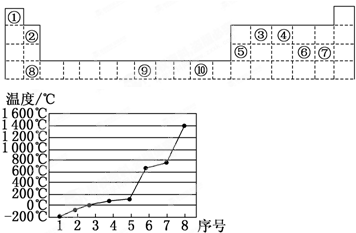
如表为周期表的一部分,其中的编号代表对应的元素.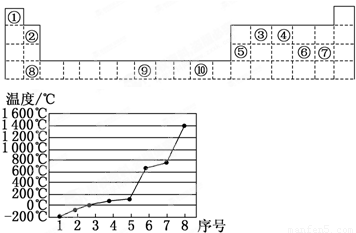
请回答下列问题:
(1)表中属于d区的元素是 (填编号).
(2)写出元素⑨的基态原子的电子排布式 .
(3)某元素的特征电子排布式为nsnnpn+1,该元素原子的核外最外层电子的成对电子为 对.
(4)第3周期8种元素按单质熔点高低的顺序如图,
其中序号“8”代表 (填元素符号);
其中电负性最大的是 (填元素符号).
【答案】分析:(1)d区元素包括ⅢB-ⅦB元素,Ⅷ族元素,为第3列到10列元素(镧系元素、锕系元素除外);
(2)由元素再周期表中的物质可知,⑨为Fe元素,属于26号元素,根据核外电子排布规律书写基态原子的电子排布式;
(3)s能级最多容纳2个电子,同一能层中s能级填满后再填充p能级,故n=2,该元素的特征电子排布式为2s2np3,据此解答;
(4)第3周期8种元素中Si是原子晶体,单质的熔点最高;
同周期自左而右电负性增强(稀有气体除外).
解答:解:(1)d区元素包括ⅢB-ⅦB元素,Ⅷ族元素,为第3列到10列元素(镧系元素、锕系元素除外),由元素在周期表中位置可知,⑨处于第8列,为第Ⅷ族元素,属于d区的元素,
故答案为:⑨;
(2)由元素再周期表中的物质可知,⑨为Fe元素,属于26号元素,基态原子的电子排布式为1S22S22P63S23P63d64S2,
故答案为:1S22S22P63S23P63d64S2;
(3)s能级最多容纳2个电子,同一能层中s能级填满后再填充p能级,故n=2,该元素的特征电子排布式为2s2np3,s能级为成对电子,p能级3个电子个占据1个轨道,故该元素原子的核外最外层电子的成对电子为1对,故答案为:1;
(4)第3周期8种元素中Si是原子晶体,单质的熔点最高;同周期自左而右电负性增强(稀有气体除外),故Cl元素的电负性最强,故答案为:Si;Cl.
点评:本题考查元素周期表的结构、核外电子排布规律、晶体结构与性质、电负性等,难度不大,整体把握元素周期表的结构,注意同周期中原子晶体的熔点最高.
(2)由元素再周期表中的物质可知,⑨为Fe元素,属于26号元素,根据核外电子排布规律书写基态原子的电子排布式;
(3)s能级最多容纳2个电子,同一能层中s能级填满后再填充p能级,故n=2,该元素的特征电子排布式为2s2np3,据此解答;
(4)第3周期8种元素中Si是原子晶体,单质的熔点最高;
同周期自左而右电负性增强(稀有气体除外).
解答:解:(1)d区元素包括ⅢB-ⅦB元素,Ⅷ族元素,为第3列到10列元素(镧系元素、锕系元素除外),由元素在周期表中位置可知,⑨处于第8列,为第Ⅷ族元素,属于d区的元素,
故答案为:⑨;
(2)由元素再周期表中的物质可知,⑨为Fe元素,属于26号元素,基态原子的电子排布式为1S22S22P63S23P63d64S2,
故答案为:1S22S22P63S23P63d64S2;
(3)s能级最多容纳2个电子,同一能层中s能级填满后再填充p能级,故n=2,该元素的特征电子排布式为2s2np3,s能级为成对电子,p能级3个电子个占据1个轨道,故该元素原子的核外最外层电子的成对电子为1对,故答案为:1;
(4)第3周期8种元素中Si是原子晶体,单质的熔点最高;同周期自左而右电负性增强(稀有气体除外),故Cl元素的电负性最强,故答案为:Si;Cl.
点评:本题考查元素周期表的结构、核外电子排布规律、晶体结构与性质、电负性等,难度不大,整体把握元素周期表的结构,注意同周期中原子晶体的熔点最高.

练习册系列答案
 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案
相关题目