题目内容
(12分)下图是一些常见的单质、化合物之间的转化关系图,有些反应中的部分物质被略去。反应①常被应用于野外焊接钢轨,②是工业上重要的反应之一。
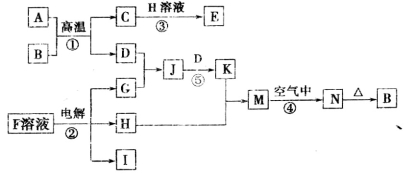
请回答下列问题:
(1)H中含有的化学键类型是________________________。
(2)上述框图所示的反应中,既属于化合反应,又属于氧化还原反应的反应共有______个;反应③的离子方程式____________________________。
(3)25℃时,以Pt为电极电解含有少量酚酞的F的饱和溶液,若在溶液变红的一极收集到0.2 g气体,则此时溶液的pH是_______(假设溶液的体积为2 L且不考虑电解后溶液体积的变化)。
(4)J溶液显_______(填“酸”、“碱”或“中”)性,原因是_________________________。(用离子方程式表示)
(12分)(1)共价键、离子键(2分)
(2)3(2分);Al2O3+2OH-+3H2O=2[Al(OH)4]- (2分)
(3)13(2分)
(4)酸(2分); Fe3++3H2O Fe(OH)3+ 3 H+(2分)
Fe(OH)3+ 3 H+(2分)
【解析】
试题分析:铝热反应常被用来焊接钢轨,所以①为铝热反应;M在空气中变为N,N受热分解,判断N是氢氧化铁,M是氢氧化亚铁,B为氧化铁,则A是Al;工业上常电解食盐水产生氯气、氢气、氢氧化钠,因为M是氢氧化亚铁,所以D为Fe,C是氧化铝;G为氯气,氯气与铁反应生成氯化铁,则J是氯化铁,K为氯化亚铁,氯化亚铁与氢氧化钠反应生成氢氧化亚铁,所以H为氢氧化钠,I是氢气,F是氯化钠,氧化铝与氢氧化钠溶液反应生成四羟基合铝酸钠 ,E是四羟基合铝酸钠。
(1)H是氢氧化钠,含有离子键和共价键;
(2)在上述反应中,铁与氯气的反应、氯化铁与铁的反应、氢氧化亚铁与氧气、水的反应都是化合反应且是氧化还原反应,共3个;反应③是氧化铝与氢氧化钠溶液反应生成四羟基合铝酸钠,离子方程式是Al2O3+2OH-+3H2O=2[Al(OH)4]-;
(3)电解饱和食盐水的化学方程式为2NaCl+2H2O 2NaOH+H2↑+Cl2↑,阴极是氢离子放电产生氢气,同时溶液变红色,所以氢气的质量是0.2g,物质的量是0.1mol,则氢氧化钠的物质的量是0.2mol,所以氢氧根离子的浓度是0.2mol/2L=0.1mol/L,则氢离子浓度是10-13mol/L,溶液的pH=13;
2NaOH+H2↑+Cl2↑,阴极是氢离子放电产生氢气,同时溶液变红色,所以氢气的质量是0.2g,物质的量是0.1mol,则氢氧化钠的物质的量是0.2mol,所以氢氧根离子的浓度是0.2mol/2L=0.1mol/L,则氢离子浓度是10-13mol/L,溶液的pH=13;
(4)J为氯化铁,铁离子的水解使溶液呈酸性,离子方程式为Fe3++3H2O Fe(OH)3+ 3 H+。
Fe(OH)3+ 3 H+。
考点:考查无机推断,物质性质的应用,离子方程式、化学方程式的书写,化学键的判断,溶液pH的计算

 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案 ABC考王全优卷系列答案
ABC考王全优卷系列答案
 C2H4(g)+4H2O(g);△H=+1411.0 kJ/mol,关于该反应,下列图示与对应的叙述相符的是
C2H4(g)+4H2O(g);△H=+1411.0 kJ/mol,关于该反应,下列图示与对应的叙述相符的是






