题目内容
某化合物6.4g在氧气中完全燃烧,只生成8.8g CO2和7.2g H2O.下列说法正确的是( )
| A、该化合物仅含碳、氢两种元素 |
| B、该化合物中碳、氢原子个数比为1:4 |
| C、无法确定该化合物是否含有氧元素 |
| D、该化合物中一定不含有氧元素 |
考点:有关有机物分子式确定的计算
专题:烃及其衍生物的燃烧规律
分析:化合物燃烧生成8.8gCO2和7.2gH2O,根据元素守恒则一定含有C、H元素,根据n=
计算二氧化碳、水的物质的量,进而计算有机物中C、H原子数目之比,根据m=nM计算C、H元素质量,根据质量守恒定律计算判断化合物中是否含有O元素.
| m |
| M |
解答:
解:化合物燃烧生成8.8gCO2和7.2gH2O,根据元素守恒则一定含有C、H元素,
8.8g二氧化碳的物质的量为
=0.2mol,n(C)=n(CO2)=0.2mol,m(C)=0.2mol×12g/mol=2.4g,
7.2g水的物质的量为
=0.4mol,n(H)=2n(H2O)=0.8mol,m(H)=0.8g,
故化合物中N(C):N(H)=0.2mol:0.8mol=1:4,
由于m(C)+m(H)=2.4g+0.8g=3.2g<6.4g,所以该化合物中一定含有氧元素,该化合物为烃的含氧衍生物,
综上分析可知,ACD错误,B正确,
故选B.
8.8g二氧化碳的物质的量为
| 8.8g |
| 44g/mol |
7.2g水的物质的量为
| 7.2g |
| 18g/mol |
故化合物中N(C):N(H)=0.2mol:0.8mol=1:4,
由于m(C)+m(H)=2.4g+0.8g=3.2g<6.4g,所以该化合物中一定含有氧元素,该化合物为烃的含氧衍生物,
综上分析可知,ACD错误,B正确,
故选B.
点评:本题考查有机物组成的确定,侧重考查质量守恒定律,题目难度不大,注意根据质量守恒判断是否含有氧元素.

练习册系列答案
相关题目
化学概念在逻辑上存在如图关系,对下列概念的说法正确的是( )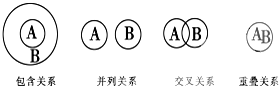

| A、化合物与电解质属于包含关系 |
| B、单质与非电解质属于包含关系 |
| C、溶液与分散系属于并列关系 |
| D、化合物与碱性氧化物属于交叉关系 |
关于△H的说法不正确的是( )
| A、反应的△H 由生成物与反应物的焓值差决定 |
| B、反应在恒压条件下的热效应为焓变 |
| C、某些反应的△H 可以通过实验测得 |
| D、放热反应的焓变取正值 |
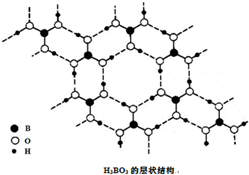 正硼酸(H3BO3)是一种片层状结构白色晶体,层内的H3BO3分子通过氢键相连(如图).下列有关说法正确的是( )
正硼酸(H3BO3)是一种片层状结构白色晶体,层内的H3BO3分子通过氢键相连(如图).下列有关说法正确的是( )| A、正硼酸晶体中只存在氢键 |
| B、H3BO3分子的稳定性与氢键有关 |
| C、分子中硼原子最外层为8电子稳定结构 |
| D、含1molH3BO3的晶体中有3mol氢键 |
除去下列物质中的杂质(括号内是杂质)所用试剂不正确的是( )
| A、NaOH溶液[Ba(OH)2]:用Na2SO4溶液 |
| B、CuO粉末[Fe粉]:用稀盐酸 |
| C、Mg粉[Al粉]:用NaOH溶液 |
| D、HNO3溶液[HCl]:用AgNO3溶液 |
下列食物属于酸性食物的是( )
| A、鸡蛋 | B、苹果 | C、葡萄 | D、西红柿 |
关于丙烯醇(CH2=CH-CH2OH)的叙述不正确的是( )
| A、可使酸性高锰酸钾褪色,反应类型为氧化反应 |
| B、一定条件下可与氢气反应生成丙醇,反应类型为加成反应 |
| C、一定条件下能与乙酸反应生成酯,反应类型为酯化反应 |
| D、该物质与乙醇属于同系物 |
在密闭容器中,在一定条件下,进行下列反应:NO(g)+CO(g)?
N2(g)+CO2(g);△H=-373.2kJ/mol,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是( )
| 1 |
| 2 |
| A、升高温度 |
| B、增大压强 |
| C、充入N2 |
| D、降低温度 |