题目内容
18.硫化钠溶于水时发生水解,其水解的离子方程式为S2-+H2O?HS-+OH-(只写第一步),在配制硫化钠 溶液时可以加入少量的NaOH以抑制其水解.分析 硫化钠是强碱弱酸盐,硫离子水解导致溶液呈碱性,为防止水解应该在配制硫化钠溶液时加入少量碱,以此解答该题.
解答 解:硫化钠是强碱弱酸盐,硫离子水解导致溶液呈碱性,水解方程式为S2-+H2O?HS-+OH-,为防止水解应该在配制硫化钠溶液时加入少量NaOH,
故答案为:S2-+H2O?HS-+OH-;NaOH.
点评 本题考查化学平衡的影响因素,侧重考查盐类水解的应用,题目难度中等,注意盐类水解的原理以及影响因素,为该题的主要考查对象,学习中注意把握.

练习册系列答案
相关题目
8.下列化合物能用相应元素的单质直接化合生成的是( )
①CuS ②FeS ③Al2S3 ④Fe2S3 ⑤Cu2S ⑥FeCl2 ⑦H2S ⑧FeCl3.
①CuS ②FeS ③Al2S3 ④Fe2S3 ⑤Cu2S ⑥FeCl2 ⑦H2S ⑧FeCl3.
| A. | ②③⑤⑦⑧ | B. | ①④⑥⑦ | C. | ①②③⑦⑧ | D. | ②③⑤⑥⑦⑧ |
9.在0.1mol•L-1氨水中加入少量的氯化铵晶体,则溶液的pH( )
| A. | 变小 | B. | 变大 | C. | 不变 | D. | 无法确定 |
13.关于浓度均为0.1 mol/L的三种溶液:①氨水、②盐酸、③氯化铵溶液,下列说法不正确的是( )
| A. | 水电离出的c(H+):②>① | |
| B. | c(NH4+):③>① | |
| C. | ①和②等体积混合后的溶液:c(H+)=c(OH- )+c(NH3•H2O) | |
| D. | ①和③等体积混合后显碱性,c(NH4+)>c(Cl-)>c(NH3•H2O ) |
3.在某无色透明的酸性溶液中,能共存的离子组是( )
| A. | Na+、Mg2+、Cl-、OH- | B. | H+、Ca2+、Na+、NO3- | ||
| C. | Cu2+、K+、SO42-、NO3- | D. | Na+、SO42-、OH-、Ca2+ |
16.下列属于热化学方程式的是( )
| A. | C+O2$\stackrel{点燃}{→}$CO2 | B. | C(s)+O2(g)$\stackrel{点燃}{→}$CO2(g)+393.5kJ | ||
| C. | C(s)+O2(g)$\stackrel{点燃}{→}$CO2(g) | D. | C(s)+O2(g)=CO2(g)+393.5kJ |
17.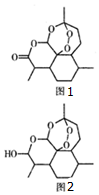 2011年9月12日,中国科学家屠呦呦获拉斯克一狄贝基临床医学研究奖,以表彰她发现了一种药物--青蒿素,它是由菊科植物在低温条件下提炼出来的一种化合物,是治疗疟疾的特效药,其结构筒式如图1所示.下列有关青蒿素的说法错误的是( )
2011年9月12日,中国科学家屠呦呦获拉斯克一狄贝基临床医学研究奖,以表彰她发现了一种药物--青蒿素,它是由菊科植物在低温条件下提炼出来的一种化合物,是治疗疟疾的特效药,其结构筒式如图1所示.下列有关青蒿素的说法错误的是( )
 2011年9月12日,中国科学家屠呦呦获拉斯克一狄贝基临床医学研究奖,以表彰她发现了一种药物--青蒿素,它是由菊科植物在低温条件下提炼出来的一种化合物,是治疗疟疾的特效药,其结构筒式如图1所示.下列有关青蒿素的说法错误的是( )
2011年9月12日,中国科学家屠呦呦获拉斯克一狄贝基临床医学研究奖,以表彰她发现了一种药物--青蒿素,它是由菊科植物在低温条件下提炼出来的一种化合物,是治疗疟疾的特效药,其结构筒式如图1所示.下列有关青蒿素的说法错误的是( )| A. | 青蒿素耐高温且易溶于水不易溶于乙醚、乙酸乙酯等有机溶剂 | |
| B. | 青蒿素分子内的1个过氧基团是对付疟原虫的核心基团 | |
| C. | 1mol青蒿素分子在碱性条件下彻底水解需消耗1mol分子水 | |
| D. | 药效比青蒿素高10倍的双氢青蒿素(见图2)化学式为C15H24O5 |
 某同学通过实验研究钠及其化合物的有关性质,请回答相关问题.
某同学通过实验研究钠及其化合物的有关性质,请回答相关问题.