题目内容
下列说法中,错误的是( )
| A、无论乙烯与Br2的加成,还是乙烯使酸性KMnO4溶液褪色,都与分子内碳碳双键有关 |
| B、用溴的四氯化碳溶液或酸性KMnO4溶液都可以鉴别乙烯和乙烷 |
| C、相同质量的乙烯和甲烷完全燃烧后产生的水的质量相同 |
| D、乙烯与乙炔都能使溴水褪色,且原理相同 |
考点:有机化学反应的综合应用
专题:有机反应
分析:A.乙烯含有碳碳双键,故能发生加成反应;乙烯中的碳碳双键具有还原性,能被酸性KMnO4溶液所氧化;
B.乙烯可与溴水发生加成反应,与酸性高锰酸钾发生氧化还原反应,乙烷性质稳定;
C.乙烯和甲烷中氢的质量分数不同;
D.乙烯含有碳碳双键,乙炔含有碳碳叁键,都能与溴水发生加成反应.
B.乙烯可与溴水发生加成反应,与酸性高锰酸钾发生氧化还原反应,乙烷性质稳定;
C.乙烯和甲烷中氢的质量分数不同;
D.乙烯含有碳碳双键,乙炔含有碳碳叁键,都能与溴水发生加成反应.
解答:
解:A.乙烯含有碳碳双键,故能发生加成反应;乙烯中的碳碳双键具有还原性,能被酸性KMnO4溶液所氧化,故A正确,
B.乙烯可与溴水发生加成反应,与酸性高锰酸钾发生氧化还原反应,可用于鉴别乙烯、乙烷,故B正确;
C.乙烯和甲烷中氢的质量分数不同,所以相同质量的乙烯和甲烷完全燃烧生成的水的质量不同,故C错误;
D.乙烯含有碳碳双键,乙炔含有碳碳叁键,都能与溴水发生加成反应,故褪色原理相同,故D正确,
故选C.
B.乙烯可与溴水发生加成反应,与酸性高锰酸钾发生氧化还原反应,可用于鉴别乙烯、乙烷,故B正确;
C.乙烯和甲烷中氢的质量分数不同,所以相同质量的乙烯和甲烷完全燃烧生成的水的质量不同,故C错误;
D.乙烯含有碳碳双键,乙炔含有碳碳叁键,都能与溴水发生加成反应,故褪色原理相同,故D正确,
故选C.
点评:本题考查了不饱和烃的性质,注意从官能团的角度来理解有机物的性质,题目较简单.

练习册系列答案
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案
相关题目
一定温度和压强不变的条件下,发生可逆反应:A(g)+3B(g)?4C(g)下列叙述能作为该反应达到平衡状态的标志的是( )
①混合气体的平均摩尔质量不再变化
②v(A):v(B):v(C)=1:3:4
③A、B、C的浓度不再变化
④C的体积分数不再变化
⑤A、B、C的分子数之比为1:3:4
⑥混合气体的密度不再变化
⑦单位时间消耗amolA,同时生成3amolB.
①混合气体的平均摩尔质量不再变化
②v(A):v(B):v(C)=1:3:4
③A、B、C的浓度不再变化
④C的体积分数不再变化
⑤A、B、C的分子数之比为1:3:4
⑥混合气体的密度不再变化
⑦单位时间消耗amolA,同时生成3amolB.
| A、②③④⑤⑥⑦ | B、③④⑦ |
| C、②③④⑦ | D、①③⑤⑥⑦ |
关于油脂的说法不正确的是( )
| A、除去试管内壁附着的油脂,可先用热碱溶液洗,再用水洗 |
| B、区别植物油和矿物油可加NaOH溶液,煮沸 |
| C、人体摄入油脂后,在体内酶的催化作用下水解为高级脂肪酸和甘油 |
| D、食用油的种类繁多,主要成份相同,仅是不同食用油添加剂成份不同而以 |
与乙炔具有相同的碳、氢百分含量,但一定既不是它的同系物又不是它的同分异构体的是( )
| A、丙炔 |
| B、乙烯 |
| C、C4H4 |
| D、苯 |
下列关于有机化合物组成与结构判断正确的是( )
| A、有机物一定都含碳、氢元素 |
| B、分子中含有羟基的化合物属于醇类 |
| C、分子式相同,各元素质量分数也相同的物质是同种物质 |
| D、有机物分子中,氢原子数不一定都是偶数 |
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A、澄清透明溶液中:Cl-、NO3-、Cu2+、NH4+ |
| B、水电离产生的c(OH-)=1×10-11mol/L的溶液:Cu2+、SO42-、NO3-、Cl- |
| C、中性溶液中:Fe3+、Al3+、NO3-、SO42- |
| D、能使苯酚变紫色的溶液:K+、Mg2+、S2-、SO42- |
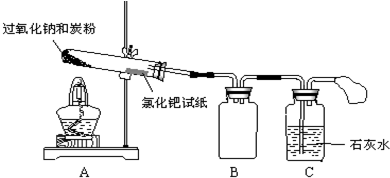
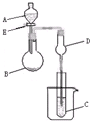 一个装置有多种用途是化学实验中经常出现的问题.用图所示装置进行实验,将A逐滴加入B中:
一个装置有多种用途是化学实验中经常出现的问题.用图所示装置进行实验,将A逐滴加入B中: