题目内容
10. 叠氮化钠(NaN3)是一种无色晶体,常见的两种制备方法为:
叠氮化钠(NaN3)是一种无色晶体,常见的两种制备方法为:2NaNH2+N2O═NaN3+NaOH+NH3,3NaNH2+NaNO3═NaN3+3NaOH+NH3↑.
回答下列问题:
(1)基NH3分子的空间构型是三角锥型;态氮原子的价层电子排布图为
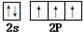 .
.(2)化合物NF3为极性分子(填“极性”或“非极性”),若其沸点为-129℃,则其晶体类型
为分子晶体.
(3)与N${\;}_{3}^{-}$互为等电子体的分子为N2O (写出一种).依据价层电子对互斥理论,NO${\;}_{3}^{-}$的空间构型为
平面三角形.
(4)氨基化钠(NaNH2)和叠氮化钠(NaN3)的晶体类型为离子晶体.
(5)已知尿素的结构式为:
 ,
,尿素分子中C和N原子的杂化方式分别是sp2、sp3
(6)安全气囊的设计原理为6NaN3+Fe2O3$\frac{\underline{\;撞击\;}}{\;}$3Na2O+2Fe+9N2↑.
①铁晶体中存在的化学键类型为金属键.
②铁晶体为体心立方堆积,其晶胞如图所示,晶胞边长为a cm,该铁晶体密度为$\frac{112}{N{\;}_{A}•a{\;}^{3}}$g•cm-3(用含a、NA
的表达式表示,其中NA为阿伏加德罗常数).
分析 (1)根据价层电子对互斥模型判断分子空间构型,N原子核外有7个电子,分别位于1s、2s、2p轨道,据此书写原子的价层电子排布图;
(2)NF3中N原子的价层电子对=3+1=4,且含有一个孤电子对,所以其空间构型为三角锥型,则分子中正负电荷中心不重合,为极性分子;
(3)将1个N原子及1个单位负电荷用O原子替换,可得其等电子体;计算NO3-中N原子价层电子对数及孤电子对,确定其空间结构;
(4)氨基化钠(NaNH2)和叠氮化钠(NaN3)都含有活泼金属元素,属于离子化合物;
(5)由尿素的结构式 可知,尿素分子中N原子成3个单键,含有1对孤对电子,杂化轨道数为4,C原子成2个C-N键、1个C=O键,没有孤对电子,杂化轨道数目为3,据此判断;
可知,尿素分子中N原子成3个单键,含有1对孤对电子,杂化轨道数为4,C原子成2个C-N键、1个C=O键,没有孤对电子,杂化轨道数目为3,据此判断;
(6)①铁晶体属于金属晶体,晶体中存在金属键;
②铁晶体为体心立方堆积,根据均摊法计算晶胞中含有2个Fe原子,结合摩尔质量计算晶胞质量,根据边长计算晶胞的体积,再根据ρ=$\frac{m}{V}$计算晶体密度.
解答 解:(1)在NH3分子中,有3个N-H键,和一对孤电子对,根据价层电子对互斥模型判断分子空间构型为三角锥型,N原子核外有7个电子,分别位于1s、2s、2p轨道,其价层电子的电子排布图为 ,故答案为:三角锥型;
,故答案为:三角锥型; ;
;
(2)NF3中N原子的价层电子对=3+1=4,且含有一个孤电子对,所以其空间构型为三角锥型,则分子中正负电荷中心不重合,为极性分子;
其沸点为-129℃,较低,根据分子晶体的性质,判断为分子晶体;
故答案为:极性;分子晶体;
(3)将1个N原子及1个单位负电荷用O原子替换,可得其等电子体为N2O等,NO3-中N原子价层电子对数=3+$\frac{5+1-2×3}{2}$=3、N原子不含孤电子对,故其空间结构为平面三角形,
故答案为:N2O;平面三角形;
(4)氨基化钠(NaNH2)和叠氮化钠(NaN3)都含有活泼金属Na元素,由阴、阳离子构成,属于离子化合物;贵答案为:离子晶体;
(5)由尿素分子的结构式 可知,尿素分子中C原子成2个C-N键、1个C=O键,没有孤对电子,杂化轨道数目为3,C原子采取sp2杂化,N原子成3个单键,含有1对孤对电子,杂化轨道数为4,N原子采取sp3杂化,
可知,尿素分子中C原子成2个C-N键、1个C=O键,没有孤对电子,杂化轨道数目为3,C原子采取sp2杂化,N原子成3个单键,含有1对孤对电子,杂化轨道数为4,N原子采取sp3杂化,
故答案为:sp2、sp3;
(6)①铁晶体属于金属晶体,晶体中存在金属键,故答案为:金属键;
②铁晶体为体心立方堆积,由其晶胞结构可知,晶胞中Fe原子数目=1+8×$\frac{1}{8}$=2,故晶胞质量=2×$\frac{56}{N{\;}_{A}}$g,晶胞边长为acm,则晶胞的体积=(a cm)3=a3 cm3,故晶体密度=$\frac{2×\frac{56}{N{\;}_{A}}}{a{\;}^{3}}$=$\frac{112}{N{\;}_{A}•a{\;}^{3}}$g•cm-3,
故答案为:$\frac{112}{N{\;}_{A}•a{\;}^{3}}$g•cm-3.
点评 本题考查了电子排布图、分子空间构型的判断、原子的杂化方式的判断等知识点,题目涉及的知识点较多,综合性较强,难度中等,注意分子空间构型的判断及原子杂化方式的判断是高考的热点.

 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案| A. | HR | B. | H2R | C. | RH4 | D. | RH3 |
| A. | CH3CH=C(CH3) CH3 3-甲基-2-丁烯 | |
| B. | CH3CH(CH3)CH(Cl)CH3 3-甲基-2-氯丁烷 | |
| C. | CH3CH(OH)CH2CH3 2-羟基丁醇 | |
| D. | CH3CH(C2H5)CH2CH2CH3 2-乙基戊烷 |
| A. | 2g H2含有的氢原子数目为NA | |
| B. | 常温常压下,22.4 LO2含有的分子数目为NA | |
| C. | 1 molZn转变为Zn2+失去的电子数目为NA | |
| D. | 1 L 1mol•L-1KOH溶液中含有的钾离子数目为NA |
| A. | 氯气与石灰乳反应制漂白粉 | B. | 钠在氯气中燃烧生成氯化钠 | ||
| C. | 氯化铵与氢氧化钙共热制氨气 | D. | 浓盐酸与二氧化锰共热制氯气 |
 ,预测该芳香烃能(填“能”或“不能”)发生该类反应.
,预测该芳香烃能(填“能”或“不能”)发生该类反应.
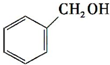 c.
c.