题目内容
下列叙述正确的是
A.25℃,某醋酸溶液的pH=a,将此溶液稀释到100倍后,溶液的pH=b,则a=b-2
B.在氨水的溶液中再加水, 将变大
将变大
C.25℃ 0.5×10-3 mol/L硫酸的pH=3.0,升高温度溶液pH增大
D.25℃,浓度为0.1 mol/L盐酸溶液,水电离出的c(H+)为0.1 mol/L
B
【解析】
试题分析:醋酸为弱酸,25℃,某醋酸溶液的pH=a,将此溶液稀释到100倍后,溶液的pH=b,则a>b-2,故A错误;氨水的溶液中再加水,促进氨水电离,故 增大,故B正确;硫酸为强酸,升高温度溶液pH不变,故C错误;浓度为0.1 mol/L盐酸溶液,
增大,故B正确;硫酸为强酸,升高温度溶液pH不变,故C错误;浓度为0.1 mol/L盐酸溶液, 由水电离的氢离子为1×10-13 mol/L,故D错误。
由水电离的氢离子为1×10-13 mol/L,故D错误。
考点:本题考查化学试剂的标志。

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
下列关于纯净物、混合物、强电解质、弱电解质和非电解质的正确组合是
纯净物 | 混合物 | 强电解质 | 弱电解质 | 非电解质 | |
A | 盐酸 | 玻璃 | 硫酸 | 氨水 | 干冰 |
B | 氢氧化钡 | 蔗糖溶液 | 硫酸钡 | 醋酸 | 水 |
C | 胆矾 | 浓硫酸 | 氧化钙 | 水 | 二氧化碳 |
D | 硝酸 | 盐酸 | 硫酸 | 醋酸 | 氢气 |
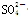 = BaSO4↓
= BaSO4↓ 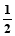 O2(g)=CO(g)△H1;C(s)+O2(g)=CO2(g) △H2
O2(g)=CO(g)△H1;C(s)+O2(g)=CO2(g) △H2
 mol
mol MnCl2 + Cl2↑ + 2H2O。取8.7g的MnO2与50mL足量的浓盐酸发生反应制取氯气。求:
MnCl2 + Cl2↑ + 2H2O。取8.7g的MnO2与50mL足量的浓盐酸发生反应制取氯气。求: