题目内容
标准状况下,将2.8g氮气、0.5mol氢气、4.0g氩气混合,该混合气体的体积是( )
| A、22.4 L |
| B、15.68 L |
| C、14.56 L |
| D、11.2 L |
考点:物质的量的相关计算
专题:计算题
分析:根据n=
计算各物质的物质的量,再根据V=nVm计算混合气体的体积.
| m |
| M |
解答:
解:标准状况下,2.8g氮气的物质的量=2.8g÷28g/mol=0.1mol,
4.0g氦气的物质的量=4.0g÷40g/mol=0.1mol,
N2、H2、Ar的物质的量分别为0.1 mol、0.5 mol、0.1 mol,n总=0.7 mol,V总=0.7 mol×22.4 L?mol-1=15.68 L,B项正确.
故选B.
4.0g氦气的物质的量=4.0g÷40g/mol=0.1mol,
N2、H2、Ar的物质的量分别为0.1 mol、0.5 mol、0.1 mol,n总=0.7 mol,V总=0.7 mol×22.4 L?mol-1=15.68 L,B项正确.
故选B.
点评:本题考查我知道的有关计算,比较基础,注意对公式的理解掌握,注意气体摩尔体积的使用条件与对象.

练习册系列答案
相关题目
现有两份等物质的量的某有机物,同温同压下使其分别与过量的Na和足量的NaHCO3反应,分别得到V1 L氢气和V2 L二氧化碳.若V1=V2≠0,则该有机物可能是( )
A、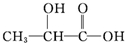 |
| B、HOOC-COOH |
| C、HOCH2CH2OH |
| D、CH3COOH |
 一种从植物中提取的天然化合物M可用于制作香水,其结构简式如图所示,该化合物中不含的官能团是( )
一种从植物中提取的天然化合物M可用于制作香水,其结构简式如图所示,该化合物中不含的官能团是( )| A、碳碳双键 | B、羟基 |
| C、醛基 | D、羰基 |
在KClO3+6HCl=KCl+3Cl2↑+3H2O中,转移的电子数目是( )
| A、5e- |
| B、10e- |
| C、6e- |
| D、12e- |
将PH试纸测定浓H2SO4的PH值,试纸的颜色将变为( )
| A、蓝 | B、黑 | C、红 | D、白? |
如图所示实验不能达到实验目的是( )
A、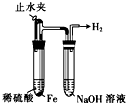 制备并观察氢氧化亚铁 |
B、 证明过氧化钠与水反应放热 |
C、 制备并收集少量NO2气体 |
D、 实验室制备少量氨气 |
在铁酸钠(Na2FeO4)对来自河湖的淡水消毒是城市饮用水处理新技术,下列对Na2FeO4用于饮用水消毒处理的分析正确的是( )
| A、Na2FeO4在溶液中显强碱性,能消毒杀菌 |
| B、在Na2FeO4中Fe为+6价,具有强氧化性,能消毒杀菌 |
| C、Na2FeO4被水还原成Fe3+,Fe3+水解为Fe(OH)3胶体,可使水中悬浮物凝聚沉降 |
| D、Na2FeO4的还原产物是Fe2+,易水解为Fe(OH)2,可使水中悬浮物凝聚沉降 |
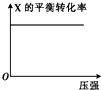 向某密闭容器中充入1mol X与2mol Y发生反应:X(g)+2Y(g)?aZ(g)△H<0,达到平衡后,改变压强,X的平衡转化率的变化如图所示.则a等于( )
向某密闭容器中充入1mol X与2mol Y发生反应:X(g)+2Y(g)?aZ(g)△H<0,达到平衡后,改变压强,X的平衡转化率的变化如图所示.则a等于( )