题目内容
在铁酸钠(Na2FeO4)对来自河湖的淡水消毒是城市饮用水处理新技术,下列对Na2FeO4用于饮用水消毒处理的分析正确的是( )
| A、Na2FeO4在溶液中显强碱性,能消毒杀菌 |
| B、在Na2FeO4中Fe为+6价,具有强氧化性,能消毒杀菌 |
| C、Na2FeO4被水还原成Fe3+,Fe3+水解为Fe(OH)3胶体,可使水中悬浮物凝聚沉降 |
| D、Na2FeO4的还原产物是Fe2+,易水解为Fe(OH)2,可使水中悬浮物凝聚沉降 |
考点:氧化还原反应,胶体的重要性质
专题:
分析:A.Na2FeO4在溶液中水解,且Fe为最高价,具有强氧化性;
B.化合物中Fe为最高价,具有强氧化性;
C.Na2FeO4不能被水还原;
D.Na2FeO4的还原产物为Fe3+.
B.化合物中Fe为最高价,具有强氧化性;
C.Na2FeO4不能被水还原;
D.Na2FeO4的还原产物为Fe3+.
解答:
解:A.Na2FeO4在溶液中水解显碱性,且Fe为最高价,具有强氧化性,能消毒杀菌,与碱性无关,故A错误;
B.化合物中Fe为最高价,具有强氧化性,则在Na2FeO4中Fe为+6价,具有强氧化性,能消毒杀菌,故B正确;
C.Na2FeO4不能被水还原,应选还原剂反应,故C错误;
D.Na2FeO4的还原产物为Fe3+,Fe3+水解为Fe(OH)3胶体,可使水中悬浮物凝聚沉降,故D错误;
故选B.
B.化合物中Fe为最高价,具有强氧化性,则在Na2FeO4中Fe为+6价,具有强氧化性,能消毒杀菌,故B正确;
C.Na2FeO4不能被水还原,应选还原剂反应,故C错误;
D.Na2FeO4的还原产物为Fe3+,Fe3+水解为Fe(OH)3胶体,可使水中悬浮物凝聚沉降,故D错误;
故选B.
点评:本题以饮用水消毒处理考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念及应用的考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
标准状况下,将2.8g氮气、0.5mol氢气、4.0g氩气混合,该混合气体的体积是( )
| A、22.4 L |
| B、15.68 L |
| C、14.56 L |
| D、11.2 L |
钨酸盐在新材料的制造中有重要应用,一种钨酸盐的制备方式如下:2GeO(g)+W2O6(g)?2GeWO4(g)△H<0.下列说法中正确的是( )
| A、增大压强可提高GeWO4的产率 |
| B、增加GeO有利于提高GeO的转化率 |
| C、实际生产中为提高经济效益要尽可能地降低反应温度 |
| D、及时分离出GeWO4可增大正反应速率 |
已知有钠、钾及钠钾合金,对于它们三者熔点高低比较正确的是( )
| A、钠钾合金>钠>钾 |
| B、钠>钾>钠钾合金 |
| C、钠>钠钾合金>钾 |
| D、钾>钠钾合金>钠 |
已知短周期元素的离子aA2+、bB+、cC2-、dD-具有相同的电子层结构.则下列叙述正确的是( )
| A、原子半径 A>B>C>D |
| B、离子半径 C2->D->B+>A2+ |
| C、原子序数 a<b<d<c |
| D、原子的失电子能力 A>B>D>C |
当周围空间不慎有大量氯气溢出时,处在该环境中的人可以用浸有一定浓度某种物质的水溶液的毛巾捂住鼻子,以防中毒,最适宜采用的物质是( )
| A、NaOH |
| B、KI |
| C、NH3?H2O |
| D、Na2CO3 |
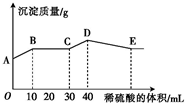 将由NaOH、BaCl2、Al2(SO4)3三种固体组成的混合物溶于足量的水中,充分溶解后,向混合溶液中滴加1mol?L-1的稀硫酸,加入稀硫酸的体积与生成沉淀的质量关系如图所示.下列有关判断正确的是( )
将由NaOH、BaCl2、Al2(SO4)3三种固体组成的混合物溶于足量的水中,充分溶解后,向混合溶液中滴加1mol?L-1的稀硫酸,加入稀硫酸的体积与生成沉淀的质量关系如图所示.下列有关判断正确的是( )| A、AB段发生反应的离子方程式为Ba2++SO42-═BaSO4↓ |
| B、BC段发生反应的离子方程式为H++OH-=H2O |
| C、D点表示的沉淀的化学式为Al(OH)3 |
| D、E点时溶液中含有AlO2- |