题目内容
在KClO3+6HCl=KCl+3Cl2↑+3H2O中,转移的电子数目是( )
| A、5e- |
| B、10e- |
| C、6e- |
| D、12e- |
考点:氧化还原反应的电子转移数目计算,氧化还原反应
专题:氧化还原反应专题
分析:化合价升高值=化合价降低值=转移电子数,据此回答.
解答:
解:反应中,氯元素的化合价从+5价降为0价,-1价升高为0价,化合价升高值=化合价降低值=转移电子数=5,
故选A.
故选A.
点评:本题考查学生氧化还原反应中电子转移和化合价升降之间的关系,难度不大.

练习册系列答案
相关题目
下列各种方法中,可制得相应金属的为( )
| A、加热氧化镁 |
| B、电解饱和氯化钠溶液 |
| C、电解熔融氯化钠 |
| D、氯化钠与铝粉高温共热 |
下面是天津大学化工学院研制的2,6-二氯苯胺的合成路线:下列说法正确的是( )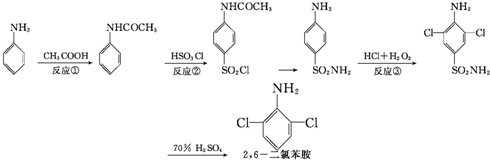

| A、反应①属于取代反应,反应②属于加成反应 |
| B、反应①属于取代反应,反应③属于氧化反应 |
| C、反应①属于取代反应,反应③属于取代反应 |
| D、反应②属于取代反应,反应③属于加成反应 |
实验室收集氯气,可供选择的方法有:①向上排空气法;②向下排空气法;③排饱和食盐水法;④排烧碱溶液法;⑤多余氯气通入水中;⑥多余氯气直接排入大气中;⑦多余氯气通入氢氧化钠溶液中;应选用的方法是( )
| A、①④⑤ | B、①③⑦ |
| C、②④⑥ | D、①③⑤ |
化学已经渗透到人类生活的各个方面,下列说法不正确的是( )
| A、臭氧可用于水体消毒,是因为臭氧能杀死水中的细菌 |
| B、明矾能水解生成氢氧化铝胶体,可用做净水剂 |
| C、食盐中添加碘酸钾,是因为碘酸钾具有氧化性 |
| D、禁止使用四乙基铅作汽油抗暴震剂,可减少汽车尾气污染 |
标准状况下,将2.8g氮气、0.5mol氢气、4.0g氩气混合,该混合气体的体积是( )
| A、22.4 L |
| B、15.68 L |
| C、14.56 L |
| D、11.2 L |
用惰性电极电解一定浓度的硫酸铜溶液,通电一段时间后,向所得的溶液中加入0.2mol Cu2(OH)2CO3后恰好恢复到电解前的浓度和pH(不考虑二氧化碳的溶解).则电解过程中共转移的电子的物质的量为( )
| A、0.4mol |
| B、0.6mol |
| C、1.2mol |
| D、1.8mol |
钨酸盐在新材料的制造中有重要应用,一种钨酸盐的制备方式如下:2GeO(g)+W2O6(g)?2GeWO4(g)△H<0.下列说法中正确的是( )
| A、增大压强可提高GeWO4的产率 |
| B、增加GeO有利于提高GeO的转化率 |
| C、实际生产中为提高经济效益要尽可能地降低反应温度 |
| D、及时分离出GeWO4可增大正反应速率 |
 工业上用CO生产燃料甲醇.一定条件下发生反应:CO(g)+2H2(g)?CH3OH(g).下图表示反应中能量的变化.
工业上用CO生产燃料甲醇.一定条件下发生反应:CO(g)+2H2(g)?CH3OH(g).下图表示反应中能量的变化.