题目内容
CO和H2的混合气体的摩尔质量为8.5g/mol,此混合气体中CO和H2的物质的量之比是 .
考点:物质的量的相关计算
专题:计算题
分析:根据混合气体的摩尔质量=
来计算.
| 总质量 |
| 总物质的量 |
解答:
解:设混合气体中CO和H2的物质的量分别是x、y,总质量是28x+2y,总物质的量是x+y,所以
=8.5,解得x:y=1:3,故答案为:1:3.
| 28x+2y |
| x+y |
点评:本题考查学生公式混合气体的摩尔质量=
的应用,难度不大.
| 总质量 |
| 总物质的量 |

练习册系列答案
 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案
相关题目
下列有关化学用语中不能体现氮原子核外电子能量有差异的是( )
A、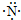 |
B、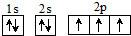 |
C、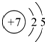 |
| D、1s22s22p3 |
甲烷的燃热为890kJ/mol,下列热化学方程式正确的是( )
| A、CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=+890kJ/mol |
| B、CH4+2O2═CO2+2H2O△H=-890kJ/mol |
| C、CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890kJ/mol |
| D、CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890kJ/mol |
将氯化铝溶液和氢氧化钠溶液等体积混合,得到的沉淀物中含铝元素的质量与溶液中含铝元素的质量相等,则原氯化铝溶液和氢氧化钠溶液的物质的量浓度之比可能是( )
①1:3 ②2:3 ③1:7 ④2:7 ⑤任意比.
①1:3 ②2:3 ③1:7 ④2:7 ⑤任意比.
| A、⑤ | B、只有① | C、②④ | D、①③ |
液氨与水相似,存在着微弱的电离:2NH3?NH4++NH2-.-50℃时,两种离子的平衡浓度均为1×10-15mol/L,下列有关液氨的离子积及其电离平衡的叙述中错误的是( )
| A、此温度下,液氨的离子积等于1×10-30 |
| B、在液氨中放人NaNH2,则液氨的离子积数值将增大 |
| C、此温度下,在液氨中加人NaNH2,则液氨中c(NH4+)<1×10-15mol/L |
| D、在液氨中加入NH4Cl,则液氨中c(NH4+)将大于c(NH2-) |
中和0.5mol H+,需要Ba(OH)2的物质的量为( )
| A、0.5mol |
| B、0.25mol |
| C、1mol |
| D、1.5mol |