题目内容
氢氧化铝既可以与酸反应又可以与碱反应,是典型的两性氢氧化物.氢氧化铝和盐酸反应的化学方程式为 ;和NaOH溶液反应的化学方程式为 .
考点:镁、铝的重要化合物
专题:元素及其化合物
分析:根据氢氧化铝的两性电离原理Al3++3OH-?Al(OH)3?AlO2-+H++H20书写化学方程式;
解答:
解:依据Al3++3OH-?Al(OH)3?AlO2-+H++H20的两性电离,故氢氧化铝和盐酸反应的化学方程式为Al(OH)3+3HCl=AlCl3+3H2O;和NaOH溶液反应的化学方程式为Al(OH)3+NaOH=NaAlO2+2H2O;
故答案:Al(OH)3+3HCl=AlCl3+3H2O;Al(OH)3+NaOH=NaAlO2+2H2O.
故答案:Al(OH)3+3HCl=AlCl3+3H2O;Al(OH)3+NaOH=NaAlO2+2H2O.
点评:本题考查学生对氢氧化铝两性知识的理解,抓住氢氧化铝的两性电离是书写方程式关键,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
1mol/L的NaCl溶液表示( )
| A、溶液中含有1molNaCl |
| B、1L溶液里含有NaCl58.5克 |
| C、58.5gNaCl溶于941.5g水中 |
| D、1molNaCl溶于1L水中 |
下列说法正确的是( )
| A、在AgNO3溶液中依次滴加同浓度的NaCl、Na2S溶液,可证明KSP(AgCl)>KSP(Ag2S) |
| B、△S>0的反应在一定条件下不一定可以自发进行 |
| C、以Al作阳极,Fe作阴极,可以实现铁上镀铝 |
| D、工业合成SO3不采用高压是因为增大压强对SO2的转化率影响不大 |
FeCl3溶液和Fe(OH)3胶体具有的共同性质是( )
| A、滴入盐酸,先产生沉淀,然后沉淀又溶解 |
| B、都能透过半透膜 |
| C、都有丁达尔现象 |
| D、都是均一的分散系 |
下列有关物质性质、应用的说法中不正确的是( )
| A、Al2O3既能溶于NaOH溶液又能溶于HCl,说明Al2O3是两性氧化物 |
| B、浓硫酸能干燥SO2、NO2等气体,说明浓硫酸具有吸水性 |
| C、SO2气体具有漂白性,通入紫色石蕊溶液中能使溶液先变红后褪色 |
| D、石英的主要成分是SiO2 |
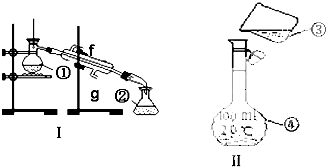
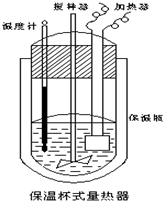 在如图所示的量热计中,将100mL 0.50mol?L-1CH3COOH溶液与100mL0.55mol?L-1NaOH 溶液混合,温度从25.0℃升高到27.7℃.已知量热计的热容常数(量热计各部件每升高1℃所需的热量)是150.5J?℃-1生成溶液的比热容为4.184J?g-1?℃-1,溶液的密度均近似为1g?mL-1.
在如图所示的量热计中,将100mL 0.50mol?L-1CH3COOH溶液与100mL0.55mol?L-1NaOH 溶液混合,温度从25.0℃升高到27.7℃.已知量热计的热容常数(量热计各部件每升高1℃所需的热量)是150.5J?℃-1生成溶液的比热容为4.184J?g-1?℃-1,溶液的密度均近似为1g?mL-1.