题目内容
科学家目前正在求证一种仅由四个中子组成的微粒,这种微粒称为“四中子”。下列关于该微粒的说法正确的是( )
| A.呈电中性 | B.带四个单位负电荷 |
| C.带四个单位正电荷 | D.质量数为2 |
A
解析试题分析:A、中子不带电,所以该微粒呈电中性,正确;B、C错误;D、质量数等于质子数与中子数的和,所以该微粒的质量数为4,错误,答案选A。
考点:考查原子结构中微粒的电性、质量数的计算

练习册系列答案
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案
相关题目
X、Y均为短周期元素,X位于ⅠA族,X、Y能形成X2Y型化合物,下列说法中正确的是( )
| A.X与Y形成的化合物中原子个数比可能为1:1 |
| B.X2Y不可能是共价化合物 |
| C.X和Y分别形成的简单离子不可能具有相同的电子层结构 |
| D.根据周期表递变规律判断,X原子半径一定大于Y原子半径 |
已知W、X、Y、Z为短周期元素,W、Z同主族,X、Y、Z同周期,W的气态氢化物的稳定性大于Z的气态氢化物的稳定性,X、Y为金属元素,X的阳离子的氧化性小于Y的阳离子的氧化性。下列说法正确的是 ( )。
| A.X、Y、Z、W的原子半径依次减小 |
| B.W与X形成的化合物中只含离子键 |
| C.W的气态氢化物的沸点一定高于Z的气态氢化物的沸点 |
| D.若W与Y的原子序数相差5,则二者形成化合物的化学式一定为Y2W3 |
在硼酸[B(OH)3]分子中,B原子与3个羟基相连,其晶体具有与石墨相似的层状结构。则分子中B原子杂化轨道的类型及同层分子间的主要作用力分别是 ( )
| A.sp,范德华力 | B.sp2,范德华力 | C.sp2,氢键 | D.sp3,氢键 |
X、Y是元素周期表中ⅦA族的两种元素,下列能说明X的非金属性比Y强的是( )。
| A.电子层数:X>Y |
| B.气态氢化物的稳定性:HX<HY |
| C.酸性:HXO4>HYO4 |
| D.能发生置换反应:Y2+2NaX=X2+2NaY |
下表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是 ( )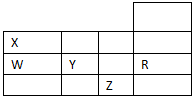
| A.常压下,五种元素的单质中,Z单质的沸点最高 |
| B.W的氢化物比X的氢化物的稳定性高 |
| C.Y、Z的阴离子电子层结构都与R原子的相同 |
| D.Y元素比W元素的非金属性强 |
原子序数为83的元素位于:①第5周期;②第6周期;③ⅣA族;④ⅤA族;⑤ⅡB族,其中正确的组合是( )。
| A.①④ | B.②③ | C.②④ | D.①⑤ |