题目内容
A、B、C是原子序数依次增大的短周期元素,A元素某种同位素原子在考古方面有重要应用,B的最外层电子是电子层数的三倍,C的焰色反应呈黄色,下列说法正确的是
A.元素A在周期表中的位置为第2周期VIA族
B.元素A、B、C的原子半径由大到小的顺序为r(C) > r(B) > r(A)
C.A、B两种元素的氢化物的稳定性A>B
D.1 molC2B2与足量的AB2完全反应转移约6.02 ×1023个电子
D
解析试题分析:根据题意知,A、B、C是原子序数依次增大的短周期元素,A元素某种同位素原子在考古方面有重要应用,则A为碳元素,B的最外层电子是电子层数的三倍,则B为氧元素,C的焰色反应呈黄色,则C为钠元素。A、A为碳元素,在周期表中的位置为第2周期ⅣA族,错误;B、根据微粒半径比较原则判断,元素A、B、C的原子半径由大到小的顺序为r(Na) > r(C)> r(O)即 r(C) > r(A)> r(B),错误;C、同一周期由左向右气态氢化物的稳定性逐渐增强,A、B两种元素的氢化物的稳定性A<B,错误,D、1 molNa2O2与足量的CO2完全反应转移约6.02 ×1023个电子,正确。
考点:考查元素推断和元素性质,元素周期律。

法国里昂的科学家发现一种只由四个中子构成的粒子,这种粒子称为“四中子”,也有人称之为“零号元素”。下列有关“四中子”粒子的说法不正确的是
| A.该粒子不显电性 | B.该粒子质量数为4 |
| C.在周期表中与氢元素占同一位置 | D.该粒子质量比氢原子大 |
俄罗斯科学家在利用回旋加速器进行的实验中,用含20个质子的钙元素的同位素反复轰击含95个质子的镅元素,结果4次成功制成4个第115号元素的原子。这4个原子在生成数微秒后衰变成第113号元素。前者的一种核素为115288X。下列有关叙述正确的是
| A.115号元素衰变成113号元素是化学变化 |
| B.核素115288X的质量数与中子数之差为173 |
| C.113号元素属于非金属元素 |
| D.115号元素的最高正化合价是 +5 |
科学家目前正在求证一种仅由四个中子组成的微粒,这种微粒称为“四中子”。下列关于该微粒的说法正确的是( )
| A.呈电中性 | B.带四个单位负电荷 |
| C.带四个单位正电荷 | D.质量数为2 |
以下说法中,不违背科学规律的是( )
①改变核外电子数可使原子与离子相互转化 ②改变核内中子数可使不同的同位素相互转化 ③改变核内质子数可使不同的元素相互转化,属于化学变化 ④改变离子的电荷数可使一种元素的阳离子转化为另一种元素的阴离子
| A.①② | B.②③ | C.③④ | D.①③ |
短周期元素X、Y、Z所在的周期数依次增大,它们的原子序数之和为20,且Y2-与Z+核外电子层的结构相同。下列化合物中同时存在极性和非极性共价键的是( )。
| A.Z2Y | B.X2Y2 | C.Z2Y2 | D.ZYX |
下列结论不正确的是 ( )
| A.微粒半径:S>S2->Cl->F |
| B.酸性:HClO4>H2SO4>H3PO4 |
| C.氧化性:Cl2>S>Se>Te |
| D.离子还原性:S2->I->Br->OH- |
元素X、Y、Z原子序数之和为36,X、Y在同一周期,X+与Z2-具有相同的核外电子层结构。下列推测不正确的是 ( )。
| A.同周期元素中X的金属性最强 |
| B.原子半径X>Y,离子半径X+>Z2- |
| C.同族元素中Z的氢化物稳定性最高 |
| D.同周期元素中Y的最高价含氧酸的酸性最强 |
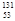 I是常规核裂变产物之一,可以通过测定大气或水中
I是常规核裂变产物之一,可以通过测定大气或水中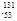 I的化学性质与
I的化学性质与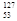 I相同
I相同