题目内容
 有一透明溶液,可能含有较多的NH4+、Mg2+、Fe3+、Al3+、Cu2+、Na+、H+、SO42-、CO32- 中的一种或几种,取此溶液做下列实验:
有一透明溶液,可能含有较多的NH4+、Mg2+、Fe3+、Al3+、Cu2+、Na+、H+、SO42-、CO32- 中的一种或几种,取此溶液做下列实验:①取少量溶液加入用盐酸酸化的BaCl2溶液,有白色沉淀生成;
②取少量原溶液加入过氧化钠粉末,溶液中有白色沉淀产生并逸出无色无味的气体,加入过氧化钠的物质的量与析出沉淀的物质的量关系如下图所示,推断:
(1)溶液中一定含有的离子是
(2)溶液中肯定不含有的离子是
(3)可能含有的离子是
考点:常见离子的检验方法
专题:离子反应专题
分析:①加入盐酸酸化的氯化钡产生白色沉淀,说明溶液中一定含有硫酸根离子;
②生成的是白色沉淀,一定没有铁离子、铁离子;根据图象分析,开始没有生成沉淀,说明溶液中一定存在氢离子,生成的沉淀只有部分溶解,证明溶液中一定存在铝离子、镁离子,能够与镁离子、铝离子反应的离子不能存在;
根据以上分析完成本题.
②生成的是白色沉淀,一定没有铁离子、铁离子;根据图象分析,开始没有生成沉淀,说明溶液中一定存在氢离子,生成的沉淀只有部分溶解,证明溶液中一定存在铝离子、镁离子,能够与镁离子、铝离子反应的离子不能存在;
根据以上分析完成本题.
解答:
解:①取少量溶液加入用盐酸酸化的BaCl2溶液,有白色沉淀生成,白色沉淀为硫酸钡,证明溶液中一定存在硫酸根离子;
②取少量原溶液加入过氧化钠粉末,溶液中有白色沉淀产生,氢氧化铁为红褐色、氢氧化铁为蓝色沉淀,所以溶液中一定不存在铜离子、铁离子;产生的无色无味的气体为氧气,氨气有刺激性气味,溶液中一定不会存在铵离子;根据图象可知,开始没有沉淀生成,证明溶液中一定存在氢离子,生成的沉淀只能部分溶解,所以溶液中一定存在铝离子和镁离子,一定不存在碳酸根离子,
(1)根据以上分析,溶液中一定存在的离子为:H+、SO42-、Al3+、Mg2+,
故答案为:H+、SO42-、Al3+、Mg2+;
(2)溶液中一定不存在的离子为:NH4+、CO32-、Cu2+、Fe3+,
故答案为:NH4+、CO32-、Cu2+、Fe3+;
(3)根据以上推断,无法确定是否含有钠离子,可以通过焰色反应检验钠离子存在情况,
故答案为:Na+;焰色反应.
②取少量原溶液加入过氧化钠粉末,溶液中有白色沉淀产生,氢氧化铁为红褐色、氢氧化铁为蓝色沉淀,所以溶液中一定不存在铜离子、铁离子;产生的无色无味的气体为氧气,氨气有刺激性气味,溶液中一定不会存在铵离子;根据图象可知,开始没有沉淀生成,证明溶液中一定存在氢离子,生成的沉淀只能部分溶解,所以溶液中一定存在铝离子和镁离子,一定不存在碳酸根离子,
(1)根据以上分析,溶液中一定存在的离子为:H+、SO42-、Al3+、Mg2+,
故答案为:H+、SO42-、Al3+、Mg2+;
(2)溶液中一定不存在的离子为:NH4+、CO32-、Cu2+、Fe3+,
故答案为:NH4+、CO32-、Cu2+、Fe3+;
(3)根据以上推断,无法确定是否含有钠离子,可以通过焰色反应检验钠离子存在情况,
故答案为:Na+;焰色反应.
点评:本题考查了离子检验方法,该题是高考中的常见题型,属于中等难度的试题,试题综合性强,难度较大,有利于培养学生的逻辑思维能力和发散思维能力,提高学生的应试能力和学习效率.

练习册系列答案
相关题目
设NA表示阿伏加德罗常数值,下列叙述正确的是( )
| A、常温常压下,56gFe与足量的盐酸完全反应转移的电子数为3NA |
| B、18gH2O中含有电子数为NA |
| C、0.1mol?L-1的硫酸铝溶液所含的SO42-数就是0.3NA |
| D、在常温、常压下,24gO2和O3的混合气体中含有的氧原子数为1.5NA? |
下列能达到实验目的是( )
A、 吸收氨气制氨水 |
B、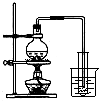 制取少量蒸馏水 |
C、 转移溶液 |
D、 除去杂质气体CO2 |
用NA表示阿伏加德罗常数的值,下列叙述中正确的是( )
| A、100mL 0.1mol?L-1的稀硫酸中含有SO42-个数为0.1NA |
| B、1molCH3+(碳正离子)中含有电子数为10NA |
| C、27g金属铝与足量的盐酸反应,铝失去电子数为3NA |
| D、12.4g白磷(分子式为P4)中含有磷原子数为1.6NA |
下列物质的贮存方法错误的是( )
| A、金属钠存放于煤油中 |
| B、硝酸贮存在避光、低温处 |
| C、氯水贮存在棕色瓶中,放在冷暗处 |
| D、烧碱溶液贮存在带玻璃塞的细口瓶中 |
电解下列物质的水溶液时,在阴极区无金属析出的是( )
| A、AgNO3 |
| B、CuCl2 |
| C、NaOH |
| D、CaCl2 |
