题目内容
反应N2(g)+3H2(g)?2NH3(g)△H<0,在其他条件不变的情况下,下列说法正确的是( )
| A、增加氮气的量,平衡正向移动,上式中△H增大 |
| B、增大压强,平衡正向移动,平衡常数增大 |
| C、升高温度,平衡逆向移动,正反应速率增大 |
| D、加入催化剂,反应速率增大,氢气转化率增大 |
考点:化学平衡的影响因素
专题:化学平衡专题
分析:A、反应一定,焓变不变;
B、反应前后气体体积减小,中等压强平衡正向进行;,平衡常数随温度变化;
C、反应是放热反应,升温平衡逆向进行,反应速率增大;
D、加入催化剂改变反应速率不改变化学平衡;
B、反应前后气体体积减小,中等压强平衡正向进行;,平衡常数随温度变化;
C、反应是放热反应,升温平衡逆向进行,反应速率增大;
D、加入催化剂改变反应速率不改变化学平衡;
解答:
解:A、反应一定,焓变不变,增加氮气的量,平衡正向移动,上式中△H不变,故A错误;
B、反应前后气体体积减小,中等压强平衡正向进行;,平衡常数随温度变化,压强改变平衡常数不变,故B错误;
C、反应是放热反应,升温平衡逆向进行,反应速率增大,正反应速率增大,故C正确;
D、加入催化剂改变反应速率不改变化学平衡,加入催化剂,反应速率增大,氢气转化率不变,故D错误;
故选C.
B、反应前后气体体积减小,中等压强平衡正向进行;,平衡常数随温度变化,压强改变平衡常数不变,故B错误;
C、反应是放热反应,升温平衡逆向进行,反应速率增大,正反应速率增大,故C正确;
D、加入催化剂改变反应速率不改变化学平衡,加入催化剂,反应速率增大,氢气转化率不变,故D错误;
故选C.
点评:本题考查了化学平衡影响因素分析判断,主要是平衡常数随温度变化分析应用,焓变和起始量和终了量有关于变化过程无关,题目较简单.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列说法或表示方法正确的是( )
| A、等物质的量的硫蒸气和硫粉分别完全燃烧,后者放出热量多 |
| B、由C(石墨)→C(金刚石)△H=+11.9kJ?mol-1可知,金刚石比石墨稳定 |
| C、在25℃,101kPa时,2g氢气完全燃烧生成液态水,放出285.8kJ热量,则氢气燃烧的热化学方程式可表示为:2H2(g)+O2(g)=2H2O(l)△H=-571.6kJ?mol-1 |
| D、H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ?mol-1,若将含0.5molH2SO4的浓硫酸与含1molNaOH的氢氧化钠溶液混合,放出的热量等于57.3kJ |
设NA为阿佛伽德罗常数,下列叙述正确的是( )
| A、28克氮气所含的氮原子数为2NA |
| B、1L1mol/L的盐酸中含有氯化氢分子为NA |
| C、标况下,11.2L水中所含的分子数为0.5NA |
| D、铁与盐酸中的反应,1mol铁失去的电子数为3NA |
下表是某浓度铬酸(H2CrO4)溶液中离子浓度(mol?L-1)与pH的关系,下列说法不正确的是( )
| pH | c(CrO
| c(HCrO
| c(Cr2O
| c(H2CrO4) | ||||||
| 4 | 0.0003 | 0.1040 | 0.4480 | 0 | ||||||
| 6 | 0.0319 | 0.0999 | 0.4370 | 0 | ||||||
| 7 | 0.2745 | 0.0860 | 0.3195 | 0 | ||||||
| 9 | 0.9960 | 0.0031 | 0.0004 | 0 |
A、铬酸第一级电离方程式为H2CrO4═H++HCrO
| ||||
| B、该铬酸溶液的物质的量浓度约为1 mol?L-1 | ||||
C、要得到CrO
| ||||
D、当电离达到平衡时,2v正(HCrO
|
“原子经济性”是“绿色化学”重要内涵.它主张在化学转化获取新物质的过程中充分利用每个原子,这样既能够充分利用资源,又能够防止污染.从“原子经济性”的角度考虑,以下转化最合理的是( )
| A、消除制硝酸工业尾气的氮氧化物污染:NO2+NO+2NaOH=2NaNO2+H2O,2NO2+2NaOH=NaNO2+NaNO3+H2O | ||||
B、制备Cu(NO3)2:2Cu+O2
| ||||
C、利用二氧化碳制造全降解塑料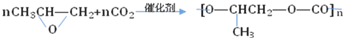 | ||||
D、用铜与浓硫酸共热制硫酸铜:Cu+2H2SO4(浓)
|
在下列溶液中,各组离子一定能够大量共存的是( )
| A、使酚酞试液变红的溶液中:Na+ Cl- SO42- Fe3+ |
| B、c(H+)=10-12mol/L的溶液:K+ Ba2+ Cl- Br- |
| C、使紫色石蕊试液变红的溶液中:Fe2+ Mg2+ NO3- Cl- |
| D、碳酸氢钠溶液:K+ SO42- Cl- H+ |
下列平衡体系,保持温度一定时,改变压强颜色会改变,但平衡并不移动,这个反应是( )
| A、2NO(g)+O2(g)?2NO2(g) |
| B、N2O4 (g)?2NO2(g) |
| C、Br2(g)+H2(g)?2HBr(g) |
| D、6NO(g)+4NH3(g)?5N2(g)+3H2O(g) |
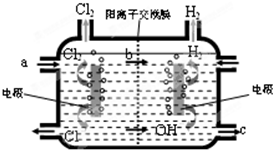 (1)已知甲醇在常温下为液体,其热值为22.7kJ?g-1,则甲醇的标准燃烧热的热化学方程式为
(1)已知甲醇在常温下为液体,其热值为22.7kJ?g-1,则甲醇的标准燃烧热的热化学方程式为