题目内容
12.25℃时,下列各组离子在指定溶液中一定能大量共存的( )| A. | 在透明的溶液中:Na+、K+、MnO4-、SO42- | |
| B. | pH>7的溶液中:Fe2+、Cu2+、SO42-、Cl- | |
| C. | 有SO42-存在的溶液中:K+、Mg2+、Ag+、NO3- | |
| D. | 加入金属铝产生H2的溶液中:NH4+、Na+、SO42-、CH3COO- |
分析 A.该组离子之间不反应;
B.pH>7的溶液,显碱性;
C.离子之间结合生成沉淀;
D.加入金属铝产生H2的溶液,为非氧化性酸或强碱溶液.
解答 解:A.该组离子之间不反应,可大量共存,故A选;
B.pH>7的溶液,显碱性,不能大量存在Fe2+、Cu2+,故B不选;
C.SO42-、Ag+结合生成沉淀,不能共存,故C不选;
D.加入金属铝产生H2的溶液,为非氧化性酸或强碱溶液,酸溶液中不能大量存在CH3COO-,碱溶液中不能大量存在NH4+,故D不选;
故选A.
点评 本题考查离子共存,为高频考点,把握习题中的信息及离子之间的反应为解答的关键,侧重分析与应用能力的考查,注意复分解反应的判断,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2.检验乙烯中的二氧化硫气体,下列试剂不能达到目的是( )
| A. | 品红溶液 | B. | 澄清石灰水 | C. | 酸性KMnO4溶液 | D. | 石蕊溶液 |
20.下列物质用加热的方法可分离的是( )
| A. | 氯化铵和消石灰固体 | B. | 碳酸氢铵和过氧化钠固体 | ||
| C. | 碘化钾和碘晶体 | D. | 硝酸钾与食盐晶体 |
7.下列化学反应所对应的离子方程式书写正确的是( )
| A. | 醋酸铵与稀盐酸反应:CH3COONH4+H+→CH3COOH+NH4+ | |
| B. | 氯化铁溶液中通入硫化氢气体:2Fe3++S2-→2Fe2++S↓ | |
| C. | 硫酸铜溶液中加入过量的氢氧化钡:Ba2++SO42-→BaSO4↓ | |
| D. | 溴化亚铁溶液中通入足量的氯气:3Cl2+2Fe2++4Br-→6Cl-+2Fe3++2Br2 |
17.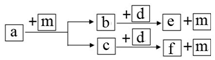 短周期元素 W、X、Y、Z 的原子序数依次递增,a、b、c、d、e、f 是由这些元素组成的化合物,d 是淡黄色粉末,m 为元素 Y 的单质,通常为无色无味的气体.上述物质的转化关系如图所示.下列说法错误的是( )
短周期元素 W、X、Y、Z 的原子序数依次递增,a、b、c、d、e、f 是由这些元素组成的化合物,d 是淡黄色粉末,m 为元素 Y 的单质,通常为无色无味的气体.上述物质的转化关系如图所示.下列说法错误的是( )
 短周期元素 W、X、Y、Z 的原子序数依次递增,a、b、c、d、e、f 是由这些元素组成的化合物,d 是淡黄色粉末,m 为元素 Y 的单质,通常为无色无味的气体.上述物质的转化关系如图所示.下列说法错误的是( )
短周期元素 W、X、Y、Z 的原子序数依次递增,a、b、c、d、e、f 是由这些元素组成的化合物,d 是淡黄色粉末,m 为元素 Y 的单质,通常为无色无味的气体.上述物质的转化关系如图所示.下列说法错误的是( )| A. | 简单离子半径:Z<Y | B. | 阴离子的还原性:Y>W | ||
| C. | 简单气态氢化物的热稳定性:Y>X | D. | W2Y2 中含有非极性键 |
4.用NA表示阿伏加德罗常数的数值.下列叙述正确的是( )
| A. | 1 mol FeI2与足量氯气反应时转移的电子数为2NA | |
| B. | 含4.9 g H2SO4与4.9 g H3PO4的混合溶液中氧原子数为0.4NA | |
| C. | 常温下,0.1 mol C2H4分子中含共用电子对数目为0.6NA | |
| D. | 25℃时,Ksp(BaSO4)=1×10-10,则BaSO4饱和溶液中Ba2+数目为1×10-5NA |
1.下列有关材料的说法错误的是( )
| A. | 铁制品在潮湿空气中更易锈蚀 | |
| B. | 二氧化硅常用于制造光导纤维 | |
| C. | 实验室中经过滤可得到纳米碳酸钙固体 | |
| D. | 聚乙烯可作食品包装材料 |