题目内容
17.下列情况会有氢气生成的是( )| A. | 铝放入冷的浓硫酸中 | B. | 铜放入热的浓硫酸中 | ||
| C. | 铝放入冷的稀酸中 | D. | 锌放入冷的稀硝酸中 |
分析 金属与弱氧化性酸(稀硫酸、盐酸)反应生成氢气,金属与强氧化性酸(浓硫酸、硝酸)反应不生成氢气,以此来解答.
解答 解:A.铝放入冷的浓硫酸中,发生钝化,开始反应生成二氧化硫,不生成氢气,故A错误;
B.铜放入热的浓硫酸中,反应生成二氧化硫,不生成氢气,故B错误;
C.铝放入冷的稀硫酸中生成硫酸铝和氢气,故C正确;
D.锌放入冷的稀硝酸中,发生氧化还原反应生成一氧化氮,不生成氢气,故D错误;
故选C.
点评 本题考查浓硫酸的性质,侧重金属与酸的反应的考查,注意酸的氧化性是解答的关键,题目难度不大.

练习册系列答案
 优学名师名题系列答案
优学名师名题系列答案
相关题目
17.除去下列溶液中的杂质(括号内是杂质)所用试剂正确的是( )
| A. | Cl2(HCl):饱和食盐水 | B. | FeCl2溶液(FeCl3):Cu | ||
| C. | NaHCO3溶液(Na2CO3):NaOH | D. | CO2(HCl ):Na2CO3溶液 |
5.将过量SO2通入下列溶液中,能出现白色浑浊的是( )
①Ca(OH)2
②BaCl2
③NaAlO2
④Na2SiO3
⑤Ba(NO3)2
⑥苯酚钠
⑦Na2CO3.
①Ca(OH)2
②BaCl2
③NaAlO2
④Na2SiO3
⑤Ba(NO3)2
⑥苯酚钠
⑦Na2CO3.
| A. | ①②④⑦ | B. | ②③⑥⑦ | C. | ④⑤⑥⑦ | D. | ③④⑤⑥ |
9.用NA表示阿伏加德罗常数的数值.下列说法正确的是( )
| A. | 0.1mol•L-1的NaOH溶液中所含Na+数目为0.1NA | |
| B. | 标准状况下,2.24L CCl4中所含的分子数为0.1NA | |
| C. | 7.8g Na2O2与足量CO2反应,转移的电子数为0.1NA | |
| D. | 常温常压下,3.2g 由O2和O3组成的混合物中所含的氧原子数为0.1NA |
 实验室里若用如图所示装置制取氨气,试用表格形式列出图中装置的错误之处,并用文字简要说明如何改正.
实验室里若用如图所示装置制取氨气,试用表格形式列出图中装置的错误之处,并用文字简要说明如何改正. ,芳香族化合物乙与甲互为同分异构体,能与NaOH溶液反应,但不能使FeCl3溶液显紫色,写出乙与NaOH溶液反应的化学方程式:
,芳香族化合物乙与甲互为同分异构体,能与NaOH溶液反应,但不能使FeCl3溶液显紫色,写出乙与NaOH溶液反应的化学方程式: +2NaOH$\stackrel{△}{→}$HCOONa+
+2NaOH$\stackrel{△}{→}$HCOONa+ +H2O.
+H2O.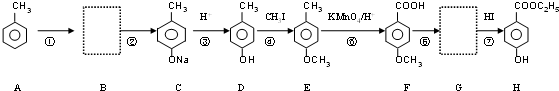
 .反应⑥的试剂和条件是乙醇、浓H2SO4.加热不能与H反应的物质是a.(选填字母)
.反应⑥的试剂和条件是乙醇、浓H2SO4.加热不能与H反应的物质是a.(选填字母)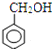 或
或 .
. .
.