题目内容
6.氧化还原反应中,水的作用可以是氧化剂、还原剂、既是氧化剂又是还原剂、既非氧化剂又非还原剂等.下列反应与Br2+SO2+2H2O═H2SO4+2HBr相比较,水的作用相同的是( )| A. | 3Fe+4H2O(g)$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2 | B. | 2Na2O2+2H2O═4NaOH+O2↑ | ||
| C. | 2H2O2═2H2O+O2↑ | D. | 2Al+2NaOH+2H2O═2NaAlO2+3H2↑ |
分析 反应Br2+SO2+2H2O=H2SO4+2HBr中,溴为氧化剂,二氧化硫为还原剂,水既不是氧化剂也不是还原剂,据此进行解答.
解答 解:A.3Fe+4H2O(g)$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2中水为氧化剂,与Br2+SO2+2H2O=H2SO4+2HBr中水的作用不相同,故A错误;
B.2Na2O2+2H2O═4NaOH+O2中水既不是氧化剂也不是还原剂,与Br2+SO2+2H2O=H2SO4+2HBr中水的作用相同,故B正确;
C.2H2O2═2H2O+O2↑水既是氧化剂也是还原剂,与Br2+SO2+2H2O=H2SO4+2HBr中水的作用不相同,故C错误;
D.2Al+2NaOH+2H2O═2NaAlO2+3H2↑中水是氧化剂,与Br2+SO2+2H2O=H2SO4+2HBr中水的作用不相同,故D错误;
故选B.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,注意从元素化合价变化的角度分析,题目难度不大.

练习册系列答案
相关题目
1.卤族元素的单质和化合物很多,我们可以利用所学物质结构与性质的相关知识去认识和理解
(1)卤族元素位于周期表的p区
(2)在不太稀的溶液中,氢氟酸是以二分子缔合(HF)2形式存在.使氢氟酸分子缔合的作用力是氢键
(3)请根据下表提供的第一电离能数据判断:理论上最有可能生成较稳定的单核阳离子的卤素原子是I(填名称或元素符号)
(4)已知高碘酸有两种形式,化学式分别为H5IO6(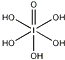 )和HIO4,前者为五元酸,后者为一元酸.请比较二者酸性强弱:H5IO6<HIO4(填“>”、“<”或“=”)
)和HIO4,前者为五元酸,后者为一元酸.请比较二者酸性强弱:H5IO6<HIO4(填“>”、“<”或“=”)
(5)已知ClO2-为V型,中心氯原子周围有四对价层电子.ClO2-中心氯原子的杂化轨道类型为sp3,写出与ClO3-互为等电子体的分子的分子式NCl3(写出1个)
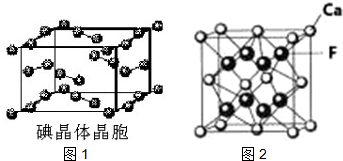
(6)如图1为碘晶体晶胞结构.有关说法中正确的是C
A.碘分子的排列有2种不同的取向,2种取向不同的碘分子以配位数4交替配位形成层结构
B.用均摊法可知平均每个晶胞中有4个碘原子
C.碘晶体为无限延伸的空间结构,是原子晶体
D.碘晶体中的碘分子间存在非极性键和范德华力
(7)已知CaF2晶体(图2)的密度为ρg/cm3,NA为阿伏加德罗常数,相邻且最近的两个Ca2+的核间距为a cm,则CaF2的相对分子质量可以表示为$\frac{\sqrt{2}}{2}$a3ρNA
(1)卤族元素位于周期表的p区
(2)在不太稀的溶液中,氢氟酸是以二分子缔合(HF)2形式存在.使氢氟酸分子缔合的作用力是氢键
(3)请根据下表提供的第一电离能数据判断:理论上最有可能生成较稳定的单核阳离子的卤素原子是I(填名称或元素符号)
| 氟 | 氯 | 溴 | 碘 | 铍 | |
| 第一电离能(kJ/mol) | 1681 | 1251 | 1140 | 1008 | 900 |
 )和HIO4,前者为五元酸,后者为一元酸.请比较二者酸性强弱:H5IO6<HIO4(填“>”、“<”或“=”)
)和HIO4,前者为五元酸,后者为一元酸.请比较二者酸性强弱:H5IO6<HIO4(填“>”、“<”或“=”)(5)已知ClO2-为V型,中心氯原子周围有四对价层电子.ClO2-中心氯原子的杂化轨道类型为sp3,写出与ClO3-互为等电子体的分子的分子式NCl3(写出1个)
(6)如图1为碘晶体晶胞结构.有关说法中正确的是C
A.碘分子的排列有2种不同的取向,2种取向不同的碘分子以配位数4交替配位形成层结构
B.用均摊法可知平均每个晶胞中有4个碘原子
C.碘晶体为无限延伸的空间结构,是原子晶体
D.碘晶体中的碘分子间存在非极性键和范德华力
(7)已知CaF2晶体(图2)的密度为ρg/cm3,NA为阿伏加德罗常数,相邻且最近的两个Ca2+的核间距为a cm,则CaF2的相对分子质量可以表示为$\frac{\sqrt{2}}{2}$a3ρNA

11.下列各组物质的关系的叙述中,正确的是( )
① 与
与  互为同系物 ②
互为同系物 ② 与
与 互为同分异构体③甲酸与硬脂酸互为同系物④甘氨酸(NH2CH2COOH)与硝基乙烷(CH3CH2NO2)互为同分异构体
互为同分异构体③甲酸与硬脂酸互为同系物④甘氨酸(NH2CH2COOH)与硝基乙烷(CH3CH2NO2)互为同分异构体
⑤C3H6与C4H8互为同系物 ⑥乙二酸与乙二醇互为同分异构体⑦淀粉与纤维素互为同分异构体.
①
 与
与  互为同系物 ②
互为同系物 ② 与
与 互为同分异构体③甲酸与硬脂酸互为同系物④甘氨酸(NH2CH2COOH)与硝基乙烷(CH3CH2NO2)互为同分异构体
互为同分异构体③甲酸与硬脂酸互为同系物④甘氨酸(NH2CH2COOH)与硝基乙烷(CH3CH2NO2)互为同分异构体⑤C3H6与C4H8互为同系物 ⑥乙二酸与乙二醇互为同分异构体⑦淀粉与纤维素互为同分异构体.
| A. | ①②④⑤ | B. | ③④⑦ | C. | ③④ | D. | ②③④⑤⑥⑦ |
18.核电荷数小于18 的某元素X,其原子的电子层数为n,最外层电子数为2n+1,原子核内质子数为2n2-1.下列有关X 的说法错误的是( )
| A. | X 能形成化学式为X(OH)3的物质 | |
| B. | X 可能形成化学式为KXO3的物质 | |
| C. | X 原子的最外层电子数一定比核电荷数少10 | |
| D. | X 可能形成化学式为KX 的物质物质 |
15.设NA为阿伏加德罗常数,下列对于0.3mol/L硫酸钾溶液的说法不正确的是( )
| A. | 1 L溶液中含有0.6 NA个钾离子 | |
| B. | 1 L溶液中含有钾离子和硫酸根离子总数为0.9 NA | |
| C. | 2 L溶液中钾离子浓度为1.2 mol/L | |
| D. | 2 L溶液中含有硫酸根离子0.6 NA个 |
 如果1mol金属R的质量为a g,密度ρ=0.97g•cm-3,请计算出每个R原子的半径的表达式(设钠为紧密堆积结构,见图).
如果1mol金属R的质量为a g,密度ρ=0.97g•cm-3,请计算出每个R原子的半径的表达式(设钠为紧密堆积结构,见图).


 .
. .
. .
.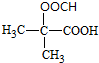 (写结构简式).
(写结构简式).