题目内容
工业上利用废铁屑(含少量氧化铝、氧化铁等)生产碱式硫酸铁[Fe(OH)SO4]的工艺流程如下:
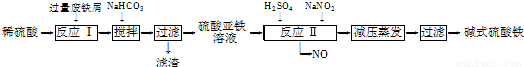
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH如下表:
沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
开始沉淀 | 2.3 | 7.5 | 3.4 |
完全沉淀 | 3.2 | 9.7 | 4.4 |
回答下列问题:
(1)流程中加入少量NaHCO3的目的是调节pH,使溶液中的___________(填“Fe3+”“Fe2+”或“Al3+”)沉淀,则调节pH的范围是___________________.
(2)在实际生产中,反应Ⅱ常同时通入O2以减少NaNO2的用量,O2与NaNO2在反应中均作______。若参与反应的O2有11.2 L(标准状况),则相当于节约NaNO2的物质的量为________。用NaNO2的缺点是产生NO污染,若用双氧水代替NaNO2发生反应的离子方程式是 。
(3)碱式硫酸铁溶于水后产生的Fe(OH)2+离子,可部分水解生成Fe2(OH)聚合离子。该水解反应的离子方程式为____________________________。
(4)在医药上常用硫酸亚铁与硫酸、硝酸的混合液反应制备碱式硫酸铁。根据我国质量标准,产品中不得含有Fe2+及NO3-。为检验所得产品中是否含有Fe2+,应使用的试剂为________(填字母)。
A. 氯水 B. KSCN溶液 C. NaOH溶液 D. 酸性KMnO4溶液
(1)Al3+ 4.4---7.5
(2)氧化剂 2mol Fe2++H2O2+2H+==Fe3++H2O
(3)2Fe(OH)2++2H2O Fe2(OH)42-+2H+
Fe2(OH)42-+2H+
(4)D
【解析】
试题分析:(1)根据题给流程分析,反应Ⅰ中稀硫酸与铁、氧化铝、氧化铁反应的生成物分别是硫酸亚铁和氢气、硫酸铝和水、硫酸铁和水;由于铁是过量的,所以生成的硫酸铁继续与铁反应生成硫酸亚铁,因此反应I溶液中存在的金属阳离子有Fe2+、Al3+。所以加入NaHCO3的目的是调节pH,使溶液中的Al3+沉淀;分析题给数据知,调节pH的范围是4.4---7.5;(2)反应II中要将亚铁离子氧化为铁离子,所以O2与NaNO2在反应中均作为氧化剂;标准状况下11.2L氧气的物质的量是0.5mol,1mol氧气在反应中得到4个电子,所以0.5mol氧气可以得到2mol电子。亚硝酸钠中氮元素的化合价是+3价,其还原产物中氮元素的化合价是+2价,得到1个电子,根据电子守恒可知,相当于是节省了2mol亚硝酸钠;用双氧水代替NaNO2发生反应的离子方程式是Fe2++H2O2+2H+==Fe3++H2O ;(3)[Fe(OH)]2+离子可部分水解生成[Fe2(OH)4]2+聚合离子,则根据电荷守恒可知一定还有氢离子生成,所以反应的离子方程式为2[Fe(OH)]2++2H2O [Fe2(OH)4]2++2H+;(4)因为产品中含有Fe3+,检验所得产品中是否含有Fe2+,可利用其还原性,应使用的试剂为酸性KMnO4溶液,选D。
[Fe2(OH)4]2++2H+;(4)因为产品中含有Fe3+,检验所得产品中是否含有Fe2+,可利用其还原性,应使用的试剂为酸性KMnO4溶液,选D。
考点:考查物质制备工艺流程的有关判断、氧化还原反应的应用与计算。

 走进文言文系列答案
走进文言文系列答案
 MnCl2+Cl2↑+2H2O。现将17.4 g MnO2投入到400 g质量分数为36.5%的浓盐酸(浓盐酸过量)中加热,充分反应后(不考虑盐酸挥发),求:
MnCl2+Cl2↑+2H2O。现将17.4 g MnO2投入到400 g质量分数为36.5%的浓盐酸(浓盐酸过量)中加热,充分反应后(不考虑盐酸挥发),求: