题目内容
标准状况下1.68L无色可燃气体在足量氧气中完全燃烧.若将产物通入足量澄清石灰水,得到的白色沉淀质量为15.0g;若用足量碱石灰吸收燃烧产物,增重9.3g.(1)计算燃烧产物中水的质量.
(2)若原气体是单一气体,通过计算推断它的分子式.
(3)若原气体是两种等物质的量的气体的混合物,其中只有一种是烃,请写出它们的分子式(只要求写出一组).
答案:
解析:
提示:
解析:
(1)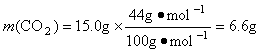
(2) 分子中C:H=1:2 n(无色可燃气体)= 分子中C原子数= 所以该气体的分子式是C2H4 (3)C4H6和H2(或C3H8和CO,C3H6和CH2O等)
|
提示:
| ①燃烧产物中与澄清石灰水反应能生成沉淀的是CO2,生成的沉淀是CaCO3,由沉淀的质量可算得CO2的质量;②碱石灰能同时吸收CO2和H2O,吸收后增加的质量是两者的总质量,从中减去CO2的质量,即是H2O的质量.第(2)小题要求推算原气体的分子式.由燃烧产物CO2和H2O可知原气体是碳氢化合物.从第(1)小题的结果,计算燃烧所得的CO2和H2O的物质的量,从而得知分子中C:H=1:2,再由试题给出的原气体在标准状况下的体积,算得它的物质的量,得出原气体1个分子中含2个C和4个H.该气体是C2H4.第(3)小题可以在第(2)小题的结果上进行推论.因为单一气体为C2H4,现为等物质的量的两种气体的混合物,即2mol该混合物应该含有4molC原子、8molH原子.由于题中限定,两种气体只有一种是烃,所以C4H8不合要求.如果一种是C4H6,则另一种为H2,符合要求.如果一种是C2H8,则另一种是C,C不是气态,可以考虑变作CO;如果一种是C3H6,则另一种是CH2(高中没有学过碳烯),不合要求,可以考虑改为CH2O、H2、CO、CH2O(甲醛)、C4H6(丁二烯或丁炔)、C3H8(丙烷)、C3H8(丙烯),都是可燃的气体.
|

练习册系列答案
相关题目

 和一个-Cl,它可能的结构有 种。(本题不考虑对映异构体)
和一个-Cl,它可能的结构有 种。(本题不考虑对映异构体)