题目内容
下列离子方程式书写正确的是( )
| A、AlCl3溶液滴加过量的氨水:Al3++4NH3?H2O═AlO2-+4NH4++H2O |
| B、硫酸和氢氧化钡溶液反应:H++SO42-+OH-+Ba2+═BaSO4↓+H2O |
| C、向氯化钙溶液中通入CO2气体:Ca2++CO2+H2O═CaCO3↓+2H+ |
| D、向氢氧化铁胶体中滴加足量HI溶液:2Fe(OH)3+6H++2I-═2Fe2++I2+6H2O |
考点:离子方程式的书写
专题:离子反应专题
分析:A.氢氧化铝不溶于氨水;
B.硫酸和氢氧化钡反应时,氢离子、氢氧根离子、水分子的计量数是2;
C.氯化钙和二氧化碳不反应;
D.氢氧化铁和碘离子发生氧化还原反应.
B.硫酸和氢氧化钡反应时,氢离子、氢氧根离子、水分子的计量数是2;
C.氯化钙和二氧化碳不反应;
D.氢氧化铁和碘离子发生氧化还原反应.
解答:
解:A.氢氧化铝不溶于氨水,离子方程式为AlCl3+3NH3?H2O=Al(OH)3↓+3NH4Cl,故A错误;
B.硫酸和氢氧化钡溶液反应为:2H++SO42-+2OH-+Ba2+=BaSO4↓+2H2O,故B错误;
C.氯化钙与二氧化碳不反应,没有离子方程式,故C错误;
D.氢氧化铁和碘离子发生氧化还原反应生成亚铁离子和碘,离子方程式为2Fe(OH)3+6H++2I-═2Fe2++I2+6H2O,故D正确;
故选D.
B.硫酸和氢氧化钡溶液反应为:2H++SO42-+2OH-+Ba2+=BaSO4↓+2H2O,故B错误;
C.氯化钙与二氧化碳不反应,没有离子方程式,故C错误;
D.氢氧化铁和碘离子发生氧化还原反应生成亚铁离子和碘,离子方程式为2Fe(OH)3+6H++2I-═2Fe2++I2+6H2O,故D正确;
故选D.
点评:本题考查了离子方程式的书写,明确离子方程式书写规则及发生的反应即可解答,根据物质的性质来分析解答,易错选项是B,注意反应计量数,为易错点.

练习册系列答案
相关题目
可逆反应A(g)+2B(g)?3C(g)+4D(g),在四种不同情况下的反应速率如下,其中反应进行得最快的是( )
| A、v(A)=0.15 mol/(L?min ) |
| B、v(B)=0.5 mol/(L?min) |
| C、v(C)=0.4 mol/(L?min) |
| D、v(D)=0.02 mol/(L?s) |
戊烷(C5H12)的同分异构体共有( )个.
| A、2个 | B、3个 | C、4个 | D、5个 |
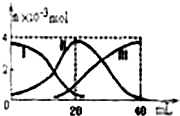 常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关微粒的物质的量变化如图(其中I代表H2A,Ⅱ代表HA-,Ⅲ代表A2-,横坐标表示加入NaOH的体积).根据图示判断,下列说法正确的是( )
常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关微粒的物质的量变化如图(其中I代表H2A,Ⅱ代表HA-,Ⅲ代表A2-,横坐标表示加入NaOH的体积).根据图示判断,下列说法正确的是( )| A、当V(NaOH)=40mL时,c(Na+)+c(H+)=2c(A2-)+c(OH-) |
| B、当V(NaOH)=20mL时,溶液中离子浓度大小关系:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-) |
| C、滴加过程中当溶液呈中性时,V(NaOH)<20mL |
| D、HA-的电离程度小于水解程度 |
下列各对物质中属于同分异构体的是( )
| A、612C和613C |
| B、O2和O3 |
| C、(CH3)2CHCH2CH3和C(CH3)4 |
| D、H2C(CH3)2和CH3CH2 CH3 |
 如图,小烧杯放在一块沾有水的玻璃片上,加入氯化铵固体与氢氧化钡晶体[Ba(OH)2?8H2O)],并用玻璃棒搅拌,玻璃片上的水结成了冰.由此可知( )
如图,小烧杯放在一块沾有水的玻璃片上,加入氯化铵固体与氢氧化钡晶体[Ba(OH)2?8H2O)],并用玻璃棒搅拌,玻璃片上的水结成了冰.由此可知( )| A、该反应中,化学能转变成热能 |
| B、反应物的总能量低于生成物的总能量 |
| C、氯化铵与氢氧化钡的反应为放热反应 |
| D、反应的热化学方程式为 2NH4Cl+Ba(OH)2→BaCl2+2NH3?H2O-Q |