题目内容
燃烧某有机物A1.50g,生成1.12L(标况)CO2和0.05molH2O,该有机物的蒸汽对空气的相对密度是1.04,求该有机物的分子式.
考点:有机物实验式和分子式的确定
专题:烃及其衍生物的燃烧规律
分析:该有机物的蒸气对空气的相对密度是1.04,空气的相对分子量为29,则该有机物的相对分子量为:29×1.04=30,1.50gA的物质的量为:n(A)=
=0.05mol;标况下1.12L二氧化碳的物质的量为0.05mol,0.9g水的物质的量为0.05mol,含有0.1mol氢原子,所以该有机物A中含有氢原子、碳原子分别为:
=1、
=2,再根据相对分子量为30可知氧原子数为1,据此进行判断.
| 1.5g |
| 30g/mol |
| 0.05mol |
| 0.05mol |
| 0.1mol |
| 0.05mol |
解答:
解:标准状况下1.12L二氧化碳的物质的量为0.05mol,0.9g水的物质的量为0.05mol,含有0.1mol氢原子;该有机物的蒸气对空气的相对密度是1.04,空气的相对分子量为29,则该有机物的相对分子量为:29×1.04=30,1.50gA的物质的量为::n(A)=
=0.05mol;标况下1.12L二氧化碳的物质的量为0.05mol,0.9g水的物质的量为0.05mol,含有0.1mol氢原子,所以该有机物A中含有氢原子、碳原子分别为:
=1、
=2,设A中含有x个O,则12+1×2+16x=30,解得x=1,所以A的分子式为:CH2O,答:该有机物的分子式为CH2O.
| 1.5g |
| 30g/mol |
| 0.05mol |
| 0.05mol |
| 0.1mol |
| 0.05mol |
点评:本题考查了常见有机物分子式的确定计算方法,题目难度中等,注意掌握确定有机物分子式的计算方法,明确相对密度与相对分子量的关系是解题关键.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
分子式为C5H12O的饱和一元醇与和它相对分子质量相同的饱和一元羧酸进行酯化反应,生成的酯共有(不考虑立体异构)( )
| A、13种 | B、14种 |
| C、15种 | D、16种 |
2013年党的十八大提出“美丽中国”的构想.水是生命之源,是“美丽中国”的重要元素,目前由于工农业的发展使水的污染有扩大的趋势.因此,我们应该掌握一些简单的净化水的方法.常见净化水的方法有①过滤、②加明矾吸附沉降、③蒸馏、④消毒杀菌.要将混有泥沙的天然水净化成生活用的自来水,应选用的方法和顺序为( )
| A、①②③④ | B、②④①③ |
| C、①③④ | D、②①④ |
下列物质的用途错误的是( )
| A、铝制容器可以贮运稀硫酸 |
| B、水玻璃可用作木材防火剂 |
| C、过氧化钠可用作潜艇供氧剂 |
| D、Fe2O3可用作红色涂料 |
下列气体能使品红溶液褪色的是( )
| A、O2 |
| B、NH3 |
| C、CO2 |
| D、SO2 |
用氟硼酸(HBF4,属于强酸)代替硫酸作铅蓄电池的电解质溶液,可使铅蓄电池在低温下工怍时的性能更优良,反应方程式为:Pb+PbO2+4HBF4
2Pb(BF4)2+2H2O,2Pb(BF4)2为可溶于水的强电解质,下列说法正确的是( )
| 放电 |
| 充电 |
| A、放电时的负极反应为:PbO2+4 H+十2e-=Pb2++2H2O |
| B、充电时,当阳极质量增加23.9 g时溶液中有0.2mo1电子通过 |
| C、放电时,正极区pH增大 |
| D、充电时,Pb电极与电源的正极相连 |
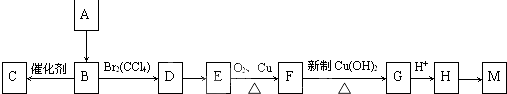
 具有复合官能团的复杂有机物:官能团具有各自的独立性,在不同条件下所发生的化学性质可分别从各官能团讨论.如:具有三个官能团分别是(填名称):
具有复合官能团的复杂有机物:官能团具有各自的独立性,在不同条件下所发生的化学性质可分别从各官能团讨论.如:具有三个官能团分别是(填名称):