题目内容
17.下列离子方程式书写正确的是( )| A. | 石灰乳与碳酸钠溶液反应:Ca2++CO32-=CaCO3↓ | |
| B. | NH4HSO3溶液与足量的氢氧化钠溶液混合加热:NH4++HSO3-+2OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+SO32-+2H2O | |
| C. | 酸性条件下KIO3溶液与KI溶液发生反应生成I2:IO3-+5I-+3H2O=3I2+6OH- | |
| D. | AgNO3溶液中加入过量的氨水:Ag++NH3•H2O=AgOH↓+NH4+ |
分析 A.石灰乳中的氢氧化钙需要保留化学式;
B.氢氧化钠溶液足量,铵根离子和亚硫酸根离子都完全反应;
C.酸性条件下,反应产物中不会存在氢氧根离子;
D.氨水过量,氢氧化银沉淀溶解.
解答 解:A.碳酸钠溶液与石灰乳的反应中,氢氧化钙不能拆开,正确的离子方程式为:CO32-+Ca(OH)2═CaCO3↓+2OH-,故A错误;
B.NH4HSO3溶液与足量的氢氧化钠溶液混合加热,反应生成氨气、亚硫酸钠和水,反应的离子方程式 为:NH4++HSO3-+2OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+SO32-+2H2O,故B正确;
C.酸性条件下KIO3溶液与KI溶液发生反应生成I2,产物中不能存在氢氧根离子,正确的离子方程式为:6H++IO3-+5I-=3I2+3H2O,故C错误;
D.AgNO3溶液中加入过量的氨水,先发生反应:Ag ++NH3•H2O=AgOH↓+NH4+,氨水过量后后发生反应:AgOH+2NH3•H2O=[Ag(NH3)2]++OH-+2H2O,不会生成沉淀,故D错误;
故选B.
点评 本题考查了离子方程式的书写,为高考的高频题,题目难度中等,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等,试题培养了学生的灵活应用基础知识的能力.

练习册系列答案
相关题目
7.当一个可逆反应进行到正反应速率与逆反应速率相等的时候,就达到了“化学平衡”.对于化学平衡的下列说法中正确的是( )
①化学反应达到化学平衡时,反应物与生成物的浓度(含量)保持不变;
②化学反应达到化学平衡时,整个反应处于停滞状态;
③平衡状态是指可逆反应在给定条件下进行的程度.
①化学反应达到化学平衡时,反应物与生成物的浓度(含量)保持不变;
②化学反应达到化学平衡时,整个反应处于停滞状态;
③平衡状态是指可逆反应在给定条件下进行的程度.
| A. | 只有① | B. | 只有①② | C. | 只有①③ | D. | ①②③ |
8.常温时,ksp(CaC2O4)=2.4×10-9,下列有关0.10mol/L草酸钠溶液的说法,正确的是( )
| A. | 溶液中各离子浓度大小关系c(Na+)>c(C2O42-)>c(OH-)>c(H+)>c(HC2O4-) | |
| B. | 若向溶液中不断加水稀释,水的电离程度增大 | |
| C. | 若用pH计测得溶液的pH=a,则H2C2O4的第二级电离平衡常数Ka2=1013-2a | |
| D. | 若向该溶液中加入等体积CaCl2溶液后能够产生沉淀,则CaCl2溶液的最小浓度应该大于2.4×10-8 mol/L |
5.下列化学用语正确的是( )
| A. | H2O2的电子式: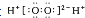 | B. | 次氯酸的结构式:H-O-Cl | ||
| C. | 中子数为10的氧原子:${\;}_8^{10}O$ | D. | 乙酸乙酯的结构简式:C4H8O2 |
12.下列关于有机化合物的叙述正确的是( )
| A. | (NH4)2SO4浓溶液和CuSO4溶液都能使蛋白质沉淀析出 | |
| B. | 苯中含有碳碳双键,其性质跟乙烯相似 | |
| C. | 乙烯使溴水褪色和苯与溴水混合振荡后水层变为无色原理相同 | |
| D. | 聚乙烯塑料的老化是由于发生了加成反应 |
2.下列有关说法正确的是( )
| A. | 糖类、油脂和蛋白质都是天然高分子化合物 | |
| B. | 煤的干馏和石油的分馏都是化学变化 | |
| C. | 苯的硝化反应属于取代反应 | |
| D. | 油脂都不能使溴的四氯化碳溶液褪色 |
6.体积为V ml,密度为ρg•mL-1的溶液,含有式量为M的溶质mg,其物质的量浓度为Cmol•L-1,质量分数为W%,下列关系中正确的是( )
| A. | $C=\frac{W×1000ρ}{M}$ | B. | $m=Vρ•\frac{W}{1000}$ | C. | $W%=\frac{CM}{100ρ}%$ | D. | $C=\frac{1000m}{VM}$ |
1.X、Y、Z是相邻主族的短周期元素,原子序数依次增大,三种元素原子的最外层电子数之和等于18,其中Y、Z同周期.下列说法正确的是( )
| A. | 离子半径:Y<Z | B. | 非金属性:X>Z | ||
| C. | 离子还原性:Y>Z | D. | 气态氢化物热稳定性:Z<X |
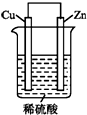 如图是Zn和Cu形成的原电池,回答下列问题:
如图是Zn和Cu形成的原电池,回答下列问题: