题目内容
1.X、Y、Z是相邻主族的短周期元素,原子序数依次增大,三种元素原子的最外层电子数之和等于18,其中Y、Z同周期.下列说法正确的是( )| A. | 离子半径:Y<Z | B. | 非金属性:X>Z | ||
| C. | 离子还原性:Y>Z | D. | 气态氢化物热稳定性:Z<X |
分析 X、Y、Z是相邻主族的短周期元素,原子序数依次增大,设中间元素最外层电子数为x,则左边的最外层电子数为x-1,右侧元素最外层电子数为x+1,因三种元素原子的最外层电子数之和等于18,即x-1+x+x+1=18,x=6,Y,Z同周期,可得:X为N元素,Y为S元素,Z为Cl.
解答 解:X、Y、Z是相邻主族的短周期元素,原子序数依次增大,设中间元素最外层电子数为x,则左边的最外层电子数为x-1,右侧元素最外层电子数为x+1,因三种元素原子的最外层电子数之和等于18,即x-1+x+x+1=18,x=6,Y,Z同周期,可得:X为N元素,Y为S元素,Z为Cl,
A、电子层数越多半径越大,相同电子层数,原子序数越小半径越大,半径S>Cl,故A错误;
B、得电子能力越强,非金属性越强,非金属性为N<Cl,故B错误;
C、单质的氧化性越强,阴离子的还原性越弱,氧化性S<Cl2,故还原性S2->Cl-,故C正确;
D、元素非金属性越强,氢化物越稳定,非金属性N<Cl,故氢化物稳定性为HCl>NH3,故D错误.
故选C.
点评 本题考查学生利用原子的结构和位置来推断元素,明确半径、金属性非金属性、离子还原性、气态氢化物稳定性的比较规律,比较基础.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
17.下列离子方程式书写正确的是( )
| A. | 石灰乳与碳酸钠溶液反应:Ca2++CO32-=CaCO3↓ | |
| B. | NH4HSO3溶液与足量的氢氧化钠溶液混合加热:NH4++HSO3-+2OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+SO32-+2H2O | |
| C. | 酸性条件下KIO3溶液与KI溶液发生反应生成I2:IO3-+5I-+3H2O=3I2+6OH- | |
| D. | AgNO3溶液中加入过量的氨水:Ag++NH3•H2O=AgOH↓+NH4+ |
18.下列关于有机化合物的结构、性质的叙述正确的是( )
| A. | 乙烯和苯都能使溴水层褪色,褪色的原因相同 | |
| B. | 淀粉、油脂、蛋白质都能水解,且都属于有机高分子化合物 | |
| C. | 蔗糖、麦芽糖的分子式均为C12H22O11,二者互为同分异构体 | |
| D. | 乙醇、乙酸均能与NaOH溶液反应,因为分子中均含有官能团“-OH” |
15.下列对应的性质描述及方程式解释均正确的是( )
| A. | 苯和溴水在铁作催化剂下发生反应: +Br$\stackrel{Fe}{→}$ +Br$\stackrel{Fe}{→}$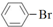 +HBr +HBr | |
| B. | 乙二醛(OHC-CHO)与银氨溶液反应:OHC-CHO+4Ag(NH3)2OH$\frac{\underline{\;\;△\;\;}}{\;}$(NH4)2C2O4+4Ag↓+2H2O+6NH3 | |
| C. | 蔗糖水解生成葡糖糖:C12H22O11+H2O$\underset{\stackrel{稀硫酸}{→}}{△}$2C6H12O6(葡糖糖) | |
| D. | 乙二醇与硬脂酸酯化可以生成硬脂酸甘油酯: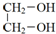 +2C17H35COOH$→_{△}^{浓硫酸}$ +2C17H35COOH$→_{△}^{浓硫酸}$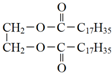 |
2.化学与生活密切相关.下列有关说法错误的是( )
| A. | 用灼烧的方法可以区分蚕丝和人造纤维 | |
| B. | 医用消毒酒精中乙醇的浓度为75% | |
| C. | 加热能杀死流感病毒是因为蛋白质受热变性 | |
| D. | 糖类、油脂和蛋白质均为高分子化合物,均可发生水解反应 |
6.真菌聚酮(X)具有多种生物活性,一定条件下可分别转化为Y和Z.
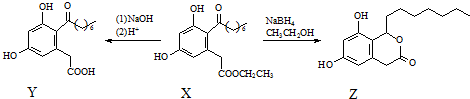
下列说法正确的是( )

下列说法正确的是( )
| A. | X、Y和Z中均不含手性碳原子 | |
| B. | Y能发生氧化、还原、取代、消去反应 | |
| C. | 一定条件下,1 mol X最多能与5 mol H2发生加成反应 | |
| D. | 1 mol Z最多可与含3 mol NaOH的溶液反应 |
10.下列各组物质中,属于同系物的是( )
| A. | CH4和 CH3Cl | B. | CH4和C3H8 | C. | C2H6和C6H12 | D. | O2和O3 |
11.下列物质与CH3CH2OH互为同系物的是( )
| A. | H-OH | B. | CH3OH | C. | C6H5OH | D. | C2H5OCH2OH |
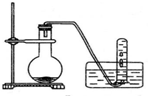 如图是铜与稀硝酸反应的实验装置,请回答下列问题:
如图是铜与稀硝酸反应的实验装置,请回答下列问题: