题目内容
下列事实不能用勒夏特列原理解释的是( )
| A、在含有Fe(SCN)3的红色溶液中加入3~5滴NaOH稀溶液,振荡静置,混合溶液颜色变浅 |
| B、把盛有NO2(g)、N2O4(g)组成的平衡体系的容器放入到热水中,混合气体的颜色加深 |
| C、反应2NO2(g)═O2(g)+2NO(g)△H<0,达到平衡后,减小压强混合气体颜色变浅 |
| D、使用催化剂可加快SO2转化为SO3的速率 |
考点:化学平衡的影响因素
专题:化学平衡专题
分析:勒沙特列原理是:如果改变影响平衡的一个条件(如浓度、压强或温度等),平衡就向能够减弱这种改变的方向移动.勒沙特列原理适用的对象应存在可逆过程,若与可逆过程无关,则不能用勒沙特列原理解释.
解答:
解:A、溶液中存在平衡Fe3++SCN-?Fe(SCN)2+,加入3~5滴NaOH稀溶液,NaOH与Fe3+反应,Fe3+浓度降低,则平衡逆向移动,溶液颜色变浅或褪去,能用勒夏特利原理来解释,故A不选;
B、NO2和N2O4存在2NO2(g)?N2O4(g)平衡,放入到热水中,温度升高,平衡逆向移动,体系颜色加深,能用勒夏特列原理解释,故B不选;
C、反应2NO2(g)═O2(g)+2NO(g)△H<0,达到平衡后,减小压强,平衡正向移动,混合气体颜色变浅,能用勒夏特列原理解释,故C不选;
D、加入催化剂能加快反应速率,但不能改变化学平衡,不能用勒夏特列原理解释,故D选;
故选:D.
B、NO2和N2O4存在2NO2(g)?N2O4(g)平衡,放入到热水中,温度升高,平衡逆向移动,体系颜色加深,能用勒夏特列原理解释,故B不选;
C、反应2NO2(g)═O2(g)+2NO(g)△H<0,达到平衡后,减小压强,平衡正向移动,混合气体颜色变浅,能用勒夏特列原理解释,故C不选;
D、加入催化剂能加快反应速率,但不能改变化学平衡,不能用勒夏特列原理解释,故D选;
故选:D.
点评:本题考查了勒夏特列原理的使用条件,难度不大,注意使用勒夏特列原理的前提必须是可逆过程.

练习册系列答案
 优加精卷系列答案
优加精卷系列答案
相关题目
某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是( )
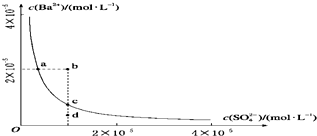

| A、加入Na2SO4可以使溶液由a点变到c点 |
| B、通过蒸发可以使溶液由d点变到c点 |
| C、b、d点都是不能长时间稳定存在的点 |
| D、a点对应的Ksp大于c点对应的Ksp |
下列物质属于弱电解质的是 ( )
| A、氯化钠 | B、蔗糖 |
| C、醋酸 | D、水玻璃 |
用NA表示阿佛加德罗常数,下列说法正确的是( )
| A、标准状态下22.4LSO3分子数为NA |
| B、常温常压下,16gO2和16gO3中所含原子数均为NA |
| C、7.8 g Na2O2含有的阴离子数是0.2NA |
| D、1L2mol?L-1的Al(NO3)3溶液中含Al3+个数为2NA |
下列说法正确的是( )
| A、在常温常压下,11.2LN2含有分子数为0.5NA |
| B、在常温常压下,22.4LNe含有原子数为NA |
| C、71gCl2所含有的原子数为2NA |
| D、在同温同压下,相同体积的气体单质含有原子数相同 |
为了研究影响化学反应速率的因素,甲、乙、丙、丁四位学生分别设计了如下四个实验,你认为不正确的是( )
| A、在相同条件下,等质量的大理石块和大理石粉与相同的盐酸反应,大理石粉反应快 |
| B、将相同大小、形状的铝条与稀硫酸和浓硫酸反应时,浓硫酸产生氢气快 |
| C、将氢气和氯气分别放在冷暗处和强光照射下,会发现光照下有氯化氢生成 |
| D、两支试管中分别加入相同条体积的双氧水,其中一支试管合在再加入少量二氧化锰,同时加热,产生氧气的快慢不同 |