题目内容
19.某有机物分子式为C4H8,核磁共振氢谱图显示该物质有两组峰,且峰面积比为3:1,该有机物的结构有几种( )| A. | 1种 | B. | 2种 | C. | 3种 | D. | 5种 |
分析 核磁共振氢谱图显示该物质有两组峰,即存在两种化学环境不同的H,峰面积比为3:1,那么H的个数分别为6和2,据此判断即可.
解答 解:C4H8的核磁共振氢谱图显示该物质有两组峰,且峰面积比为3:1,那么分子中H原子的个数分别为6和2,结构简式可以是CH3CH=CHCH3和CH2=C(CH3)2,总共有2种,故选B.
点评 本题主要考查的是有机化合物的同分异构体的判断,涉及核磁共振氢谱的知识,难度不大.

练习册系列答案
相关题目
10.下列反应既是氧化还原反应,又是吸热反应的是( )
| A. | 铝片与稀H2SO4反应 | B. | Ba(OH)2•8H2O与NH4Cl反应 | ||
| C. | 甲烷在空气中燃烧 | D. | 加热条件下H2与CuO反应 |
7.短周期元素X、Y、Z、W在周期表中的位置关系如表所示,已知在同周期元素的常见简单离子中,W的简单离子半径最小,X、Y、Z、W的单质及其化合物在日常生活中用途极其广泛.
 (1)X、Y、Z元素的氢化物均有两种或两种以上,其中一定条件下,液态YH3与液态H2Z可以发生类似方式电离,则液态YH3中阴离子的电子式为
(1)X、Y、Z元素的氢化物均有两种或两种以上,其中一定条件下,液态YH3与液态H2Z可以发生类似方式电离,则液态YH3中阴离子的电子式为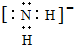 .
.
(2)某汽车尾气分析仪以燃料电池为工作原理测定XZ的浓度,其装置如图所示,该电池中电解质为氧化钇-氧化钠,其中Z2-可以在固体介质NASICON中自由移动.则负极的反应式CO-2e-+O2-═CO2.
(3)关于该电池的下列说法,正确的是AC.
A.工作时电极b作正极,Z2-通过固体介质NASICON由电极b流向电极a
B.工作时电流由电极a通过传感器流向电极b
C.传感器中通过的电流越大,尾气中XZ的含量越高.
| X | Y | Z | |
| W |
 (1)X、Y、Z元素的氢化物均有两种或两种以上,其中一定条件下,液态YH3与液态H2Z可以发生类似方式电离,则液态YH3中阴离子的电子式为
(1)X、Y、Z元素的氢化物均有两种或两种以上,其中一定条件下,液态YH3与液态H2Z可以发生类似方式电离,则液态YH3中阴离子的电子式为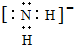 .
.(2)某汽车尾气分析仪以燃料电池为工作原理测定XZ的浓度,其装置如图所示,该电池中电解质为氧化钇-氧化钠,其中Z2-可以在固体介质NASICON中自由移动.则负极的反应式CO-2e-+O2-═CO2.
(3)关于该电池的下列说法,正确的是AC.
A.工作时电极b作正极,Z2-通过固体介质NASICON由电极b流向电极a
B.工作时电流由电极a通过传感器流向电极b
C.传感器中通过的电流越大,尾气中XZ的含量越高.
14.在元素周期表中位于金属元素和非金属元素交界处最容易找到的材料是( )
| A. | 制催化剂的材料 | B. | 半导体材料 | ||
| C. | 制农药的材料 | D. | 耐高温、耐腐蚀的合金材料 |
4.下列说法不正确的是( )
| A. | 不能自发进行的氧化还原反应,也可以通过电解来实现 | |
| B. | 电解质溶液导电是化学变化,金属导电是物理变化 | |
| C. | 电解池和原电池中均发生氧化还原反应 | |
| D. | 电解、电离、原电池均需要通电 |
11.下列排列顺序正确的是( )
①热稳定性:H2O>HF>H2S
②原子半径:Na>Mg>O
③酸性:H3PO4>H2SO4>HClO4
④离子半径:r(Na)<r(Cl)<r(S).
①热稳定性:H2O>HF>H2S
②原子半径:Na>Mg>O
③酸性:H3PO4>H2SO4>HClO4
④离子半径:r(Na)<r(Cl)<r(S).
| A. | ①③ | B. | ②④ | C. | ①④ | D. | ②③ |
8.化学已经渗透到人类生活的各个方面,下列说法正确的是( )
| A. | 高纯度的硅单质广泛用于制作光导纤维,光导纤维遇强碱会“断路” | |
| B. | 氮的固定只有在高温、高压、催化剂的条件下才能实现 | |
| C. | 服用铬含量超标的药用胶囊会对人体健康不会造成危害 | |
| D. | 高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,既能杀菌消毒又能净水 |

 $→_{Ⅱ}^{一定条件}$Y$→_{Ⅲ}^{一定条件}$乙
$→_{Ⅱ}^{一定条件}$Y$→_{Ⅲ}^{一定条件}$乙 +HCl$\stackrel{一定条件}{→}$
+HCl$\stackrel{一定条件}{→}$ (不需要注明反应条件)
(不需要注明反应条件)
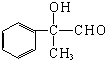 ;丙的结构简式为
;丙的结构简式为 .
.