题目内容
在呼吸面具和潜水艇中可用过氧化钠作为供氧剂.请选用适当的化学试剂和实验用品,用如图中的实验装置进行实验,证明过氧化钠可作供氧剂.
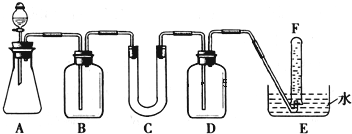
(1)A是利用盐酸和石灰石制取CO2的装置,A中发生反应的化学方程式为 .
(2)填写表中空格:
(3)写出过氧化钠与二氧化碳反应的化学方程式: ,
标准状况下将少量二氧化碳通入足量过氧化钠中充分反应后,过氧化钠增重5.6g,则通入二氧化碳的体积为 L.
(4)试管F中收集满气体后,先把E中的导管移出水面,关闭分液漏斗的活塞,用拇指堵住试管口,取出试管,下一步实验操作是: .

(1)A是利用盐酸和石灰石制取CO2的装置,A中发生反应的化学方程式为
(2)填写表中空格:
| 仪器 | 加入试剂 | 加入该试剂的目的 |
| B | 饱和NaHCO3溶液 | |
| C | ||
| D |
标准状况下将少量二氧化碳通入足量过氧化钠中充分反应后,过氧化钠增重5.6g,则通入二氧化碳的体积为
(4)试管F中收集满气体后,先把E中的导管移出水面,关闭分液漏斗的活塞,用拇指堵住试管口,取出试管,下一步实验操作是:
考点:碱金属及其化合物的性质实验
专题:实验题,元素及其化合物
分析:由实验装置可知,本实验首先由CaCO3和盐酸反应生成CO2,产生气体通过饱和NaHCO3溶液,以除去CO2气体中混入的HCl,然后过氧化钠与CO2和水气反应,产生O2,用排水法收集O2,最后取出试管,立即把带火星的木条伸入试管口内,木条复燃,证明试管中收集的气体是氧气.
解答:
解:(1)A为由CaCO3和盐酸反应生成CO2,方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑,
故答案为:CaCO3+2HCl=CaCl2+H2O+CO2↑;
(2)产生气体通过饱和NaHCO3溶液,以除去CO2气体中混入的HCl,然后过氧化钠与CO2和水气反应,产生O2,由于生成的氧气中混有二氧化碳气体,应用NaOH溶液洗气,吸收未反应的CO2气体,用排水法收集O2,
故答案为:
(3)过氧化钠与二氧化碳反应生成碳酸钠和氧气,反应的化学方程式为2Na2O2+2CO2=2Na2CO3+O2,标准状况下将少量二氧化碳通入足量过氧化钠中充分反应后,过氧化钠增重5.6g,依据反应2Na2O2+2CO2=2Na2CO3+O2,增加的质量即为增加的CO的质量,n(CO2)=n(CO)=
=0.2mol,即体积为0.2mol×22.4L/mol=4.48L,故答案为:2Na2O2+2CO2=2Na2CO3+O2,4.48L;
(4)本实验的目的为证明过氧化钠可作供氧剂,收集气体后要验证是否为氧气,为防止倒吸,应先把E中的导管移出水面,然后关闭分液漏斗活塞,用带火星的木条伸入试管口内,木条复燃,证明试管中收集的气体是氧气,
故答案为:立即把带火星的木条伸入试管口内,木条复燃,证明试管中收集的气体是氧气.
故答案为:CaCO3+2HCl=CaCl2+H2O+CO2↑;
(2)产生气体通过饱和NaHCO3溶液,以除去CO2气体中混入的HCl,然后过氧化钠与CO2和水气反应,产生O2,由于生成的氧气中混有二氧化碳气体,应用NaOH溶液洗气,吸收未反应的CO2气体,用排水法收集O2,
故答案为:
| 仪器 | 加入试剂 | 加入该试剂的目的 |
| B | 饱和NaHCO3溶液 | 除去CO2气体中混入的HCl |
| C | 过氧化钠 | 与CO2和水气反应,产生O2 |
| D | NaOH溶液 | 吸收未反应的CO2气体 |
| 5.6g |
| 28g/mol |
(4)本实验的目的为证明过氧化钠可作供氧剂,收集气体后要验证是否为氧气,为防止倒吸,应先把E中的导管移出水面,然后关闭分液漏斗活塞,用带火星的木条伸入试管口内,木条复燃,证明试管中收集的气体是氧气,
故答案为:立即把带火星的木条伸入试管口内,木条复燃,证明试管中收集的气体是氧气.
点评:本题考查过氧化钠的性质的实验设计,题目难度不大,解答本题注意把握实验原理和相关实验的基本操作,注意除杂的先后顺序和检验氧气的操作方法.

练习册系列答案
 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案
相关题目
下列有关原子、分子的说法错误的是( )
| A、原子、分子都是构成物质的微粒 |
| B、原子、分子总在不断运动 |
| C、分子可以再分,原子不能再分 |
| D、分子间有一定的间隔 |
甲、乙、丙、丁四种物质中,甲、乙、丙均含有相同的某种元素,它们之间具有如图转化关系:甲
乙
丙.下列有关物质的推断不正确的是( )
| 丁 |
| 丁 |
| 甲 |
| A、若甲为焦炭,则丁可能是O2 |
| B、若甲为NaAlO2,则丁可能是盐酸 |
| C、若甲为NaOH溶液,则丁可能是CO2 |
| D、若甲为Fe,则丁可能是盐酸 |
下列有关实验的说法正确的是( )
| A、实验室配制FeCl3溶液时加入铁粉和稀盐酸 |
| B、为测定熔融氢氧化钠的导电性,可在瓷坩埚中熔化氢氧化钠固体后进行测量 |
| C、除去铁粉中混有少量铝粉,可加入过量的氢氧化钠溶液,完全反应后过滤 |
| D、某溶液中加入盐酸能产生使澄清石灰水变浑浊的气体,该溶液中一定含有CO32- |
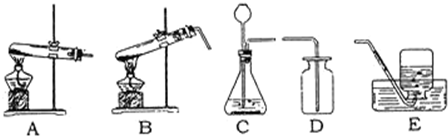
 工业纯碱中常含有NaCl、Na2SO4等杂质,为了测定工业纯碱中Na2CO3的含量,某同学设计了如图装置:
工业纯碱中常含有NaCl、Na2SO4等杂质,为了测定工业纯碱中Na2CO3的含量,某同学设计了如图装置: