题目内容
16.将等物质的量的①Na②Na2O③Na2O2④NaOH露置于空气中,最后全变成Na2CO3,质量变化由小到大的顺序是( )| A. | ④<③<①<② | B. | ②<①<③<④ | C. | ④<②<③<① | D. | ③<④<②<① |
分析 各物质暴露在空气中,最终都转化为Na2CO3,各物质的量相等,设都是2mol,由钠元素守恒,据此判断.
解答 解:①Na变成碳酸钠,质量变化为60g; ②Na2O变成碳酸钠,质量变化为44×2=88g;③Na2O2变成碳酸钠,质量变化为28×2=56g;④NaOH变成碳酸钠,质量变化为28-2=26g,所以质量变化由小到大的顺序是④<③<①<②,
故选A.
点评 本题考查钠元素单质化合物性质、化学计算等,注意利用钠元素守恒解答,结合化学式质量分数比较判断,避免计算的繁琐.

练习册系列答案
相关题目
6.合成导电高分子材料PPV的反应:
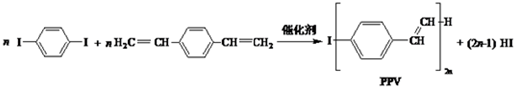
下列说法正确的是( )

下列说法正确的是( )
| A. | 合成PPV的反应为缩聚反应 | |
| B. | PPV与聚苯乙烯具有相同的重复结构单元 | |
| C. | 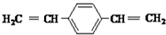 和苯乙烯互为同系物 和苯乙烯互为同系物 | |
| D. | 通过红外光谱测定PPV的平均相对分子质量,可得其聚合度 |
7.下列有关糖类、油脂和蛋白质的叙述正确的是( )
| A. | 油脂的水解反应又叫做皂化反应 | |
| B. | 糖类都能发生水解反应 | |
| C. | 蛋白质发生变性后,生成氨基酸 | |
| D. | 通过灼烧时产生的气味可以鉴别蚕丝和棉纱 |
11.X、Y、Z、W为四种短周期主族元素,它们在周期表中的位置如图所示.Z元素原子核外K层与M层电子数相等.下列说法中正确的是( )
| X | Y | ||
| Z | W |
| A. | 与同浓度的盐酸反应,Z比W更剧烈 | |
| B. | 原子半径由小到大的顺序为:X<Z<Y<W | |
| C. | Y元素最高价氧化物对应的水化物的化学式为H3YO4 | |
| D. | X、Z两种元素的氧化物中所含化学键类型相同 |
4.下列有关叙述正确的是( )
| A. | 室温下,将等浓度等体积的NaHSO4和Ba(OH)2溶液混合并充分反应后的溶液中:c(Ba2+)+c(Na+)+c(H+)=c(SO42-)+c(OH-) | |
| B. | 向甲苯中滴加少量浓溴水并振荡静置,溶液分层且下层近无色,是因为发生了取代反应 | |
| C. | 可用稀盐酸酸化的BaCl2检验Na2SO3和Na2S2O3的混合液中是否混有Na2SO4 | |
| D. | 在与Al作用产生气体的溶液中一定不存在的离子组有:NO3-、Cl-、Na+、Mg2+ |
1.下列说法错误的是( )
| A. | 硝酸与铁反应可产生H2 | |
| B. | 浓硫酸可用于干燥O2、CO2 | |
| C. | 不可将水直接导入浓硫酸里进行稀释 | |
| D. | 浓硫酸对皮肤或者衣物有很强的腐蚀性 |
2.若NA仅为阿伏加德罗常数的数值.下列说法正确的是( )
| A. | 1.0L0.1mol•L-1NH4Cl溶液中NH4+的个数为0.1NA | |
| B. | 1molNa2O和Na2O2固体中含有的阴、阳离子总数为3NA | |
| C. | 标准状况下,2.24LCl2完全溶于水转移的电子数目为0.1NA | |
| D. | 标准状况下,11.2LCH3COOH中含有的C-H键数目为1.5NA |