题目内容
11.X、Y、Z、W为四种短周期主族元素,它们在周期表中的位置如图所示.Z元素原子核外K层与M层电子数相等.下列说法中正确的是( )| X | Y | ||
| Z | W |
| A. | 与同浓度的盐酸反应,Z比W更剧烈 | |
| B. | 原子半径由小到大的顺序为:X<Z<Y<W | |
| C. | Y元素最高价氧化物对应的水化物的化学式为H3YO4 | |
| D. | X、Z两种元素的氧化物中所含化学键类型相同 |
分析 X、Y、Z、W为四种短周期主族元素,Z元素原子核外K层与M层电子数相等,则Z原子M层电子数为2,故Z为Mg元素;由元素周期表中的相对位置可知,W为Al元素、X为C元素、Y为N元素,结合对应单质、化合物的性质以及元素周期律知识解答该题.
解答 解:X、Y、Z、W为四种短周期主族元素,Z元素原子核外K层与M层电子数相等,则Z原子M层电子数为2,故Z为Mg元素,由元素周期表中的相对位置可知,W为Al元素、X为C元素、Y为N元素,
A.金属性:Mg>Al,则与同浓度的盐酸反应,Mg比铝更剧烈,故A正确;
B.同周期自左而右原子半径减小,同主族自上而下原子半径增大,故原子半径大小为:N<C<Al<Mg,故B错误;
C.Y为N元素,最高价氧化物对应的水化物化学式为HNO3,故C错误;
D.X、Z两种元素的氧化物分别为二氧化碳和氧化镁,分别含有共价键、离子键,故D错误;
故选A.
点评 本题考查原子结构与元素周期律,为高频考点,把握原子结构、电子排布推断元素等为解答的关键,侧重分析与应用能力的考查,注意元素周期律的应用,题目难度不大.

练习册系列答案
相关题目
19. 把在空气中久置的铝片5.0g投入盛有50mL 0.1mol•L-1盐酸溶液的烧杯中,该铝片与盐酸反应,产生氢气的速率v(H2)与反应时间t的关系,可用如图所示的坐标曲线来表示,下列推论错误的是( )
把在空气中久置的铝片5.0g投入盛有50mL 0.1mol•L-1盐酸溶液的烧杯中,该铝片与盐酸反应,产生氢气的速率v(H2)与反应时间t的关系,可用如图所示的坐标曲线来表示,下列推论错误的是( )
 把在空气中久置的铝片5.0g投入盛有50mL 0.1mol•L-1盐酸溶液的烧杯中,该铝片与盐酸反应,产生氢气的速率v(H2)与反应时间t的关系,可用如图所示的坐标曲线来表示,下列推论错误的是( )
把在空气中久置的铝片5.0g投入盛有50mL 0.1mol•L-1盐酸溶液的烧杯中,该铝片与盐酸反应,产生氢气的速率v(H2)与反应时间t的关系,可用如图所示的坐标曲线来表示,下列推论错误的是( )| A. | O→a段不产生氢气是因为表面的氧化物隔离了铝和稀盐酸 | |
| B. | b→c段产生氢气的速率增加较快的主要原因之一是温度升高 | |
| C. | t=c时刻,反应处于平衡 | |
| D. | t>c时,产生氢气的速率降低的主要原因是溶液中H+浓度下降 |
6.下列哪一个分子模型不属于比例模型( )
| A. | 甲烷分子 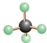 | B. | 乙醇分子 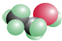 | C. | 苯分子  | D. | 乙烯分子 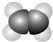 |
16.将等物质的量的①Na②Na2O③Na2O2④NaOH露置于空气中,最后全变成Na2CO3,质量变化由小到大的顺序是( )
| A. | ④<③<①<② | B. | ②<①<③<④ | C. | ④<②<③<① | D. | ③<④<②<① |
17.去甲肾上腺素可以调控动物机体的植物性神经功能.其结构简式如图所示.下列说法正确的是( )

| A. | 每个去甲肾上腺素分子中含有 3 个酚羟基 | |
| B. | 去甲肾上腺素分子难溶于水 | |
| C. | 1mol去甲肾上腺素最多能与2molBr2发生取代反应 | |
| D. | 去甲肾上腺素既能与盐酸反应,又能与氢氧化钠溶液反应 |