题目内容
20.下列反应的离子方程式正确的是( )| A. | 大理石溶于醋酸的反应:CaCO3+2CH3COOH═Ca2++2CH3COO-+CO2↑+H2O | |
| B. | 实验室制取CO2:CO32-+2H+═CO2↑+H2O | |
| C. | 铁和硝酸银溶液反应:Fe+Ag+═Ag+Fe2+ | |
| D. | Ca(HCO3)2溶液中加入过量KOH溶液:Ca2++HCO3-+OH-═CaCO3↓+H2O |
分析 A.反应生成醋酸钙、水、二氧化碳;
B.利用碳酸钙与盐酸反应制备;
C.电子、电荷不守恒;
D.反应生成碳酸钙、碳酸钾、水.
解答 解:A.大理石溶于醋酸的反应的离子反应为CaCO3+2CH3COOH═Ca2++2CH3COO-+CO2↑+H2O,故A正确;
B.实验室制取CO2的离子反应为CaCO3+2H+═Ca2++CO2↑+H2O,故B错误;
C.铁和硝酸银溶液反应的离子反应为Fe+2Ag+═2Ag+Fe2+,故C错误;
D.Ca(HCO3)2溶液中加入过量KOH溶液的离子反应为Ca2++2HCO3-+2OH-═CO32-+CaCO3↓+2H2O,故D错误;
故选A.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重分析与应用能力的考查,注意离子反应中保留化学式的物质及离子反应中电子、电荷守恒,题目难度不大.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案
相关题目
11.在稀硫酸中加入铜粉,铜粉不溶,再加入下列物质:①FeCl3;②Fe2O3;③Cu(NO3)2;④KNO3,铜粉溶解的是( )
| A. | 只有①或② | B. | 只有②或④ | ||
| C. | 只有①或②或③ | D. | 上述四种物质中任意一种 |
8.下列实验中均需要的仪器是( )
①蒸发 ②配制溶液 ③过滤.
①蒸发 ②配制溶液 ③过滤.
| A. | 试管 | B. | 玻璃棒 | C. | 胶头滴管 | D. | 漏斗 |
5.下列电子式中,不正确的是( )
| A. | 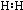 | B. |  | C. | 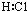 | D. | 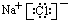 |
12.短周期元素X、Y、Z、M、N原子序数依次增大,有关信息如下表:
(1)XY2的电子式是 ;Z2Y2中所含化学键类型是离子键和非极性共价键;XY2与Z2Y2反应的化学方程式是2CO2+2Na2O2=2Na2CO3+O2.
;Z2Y2中所含化学键类型是离子键和非极性共价键;XY2与Z2Y2反应的化学方程式是2CO2+2Na2O2=2Na2CO3+O2.
(2)X的非金属性比M强(填“强”或“弱”),能证明此结论的事实是CO2+H2O+SiO32-=H2SiO3↓+CO32-或2CO2+2H2O+SiO32-=H2SiO3↓+2HCO3-(用离子方程式表示).
| 元素 | 有关信息 |
| X | 最外层电子数是次外层的2倍 |
| Y | 元素主要化合价为-2价 |
| Z | 其单质及化合物的焰色为黄色 |
| M | 与X同主族,其单质为半导体材料 |
| N | 其单质在Y单质中燃烧,发出明亮的蓝紫色火焰 |
 ;Z2Y2中所含化学键类型是离子键和非极性共价键;XY2与Z2Y2反应的化学方程式是2CO2+2Na2O2=2Na2CO3+O2.
;Z2Y2中所含化学键类型是离子键和非极性共价键;XY2与Z2Y2反应的化学方程式是2CO2+2Na2O2=2Na2CO3+O2.(2)X的非金属性比M强(填“强”或“弱”),能证明此结论的事实是CO2+H2O+SiO32-=H2SiO3↓+CO32-或2CO2+2H2O+SiO32-=H2SiO3↓+2HCO3-(用离子方程式表示).
9.卤代烃能够发生下列反应:2CH3CH2Br+2Na→CH3CH2CH2CH3+2NaBr,下列有机物不可能合成环状烷的是( )
| A. | BrCH2CH2CH2CH2CH2Br | B. | 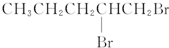 | ||
| C. | 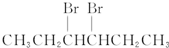 | D. | CH3CH2CH2CH2CH2Br |
 A、B、C、X是中学化学常见物质,均由短周期元素组成,转化关系如图所示.请针对以下不同情况回答:
A、B、C、X是中学化学常见物质,均由短周期元素组成,转化关系如图所示.请针对以下不同情况回答: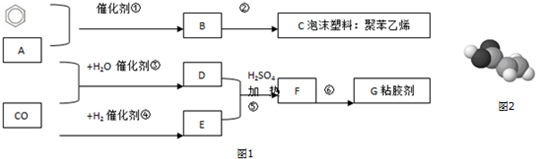

 .
.