题目内容
12.对于反应C(s)+H2O(g)?CO(g)+H2(g);△H>0,下列有关说法正确的是( )| A. | 升高体系温度,平衡常数K减小 | |
| B. | 增大体系压强,平衡常数K不发生变化 | |
| C. | 平衡常数表达式为K=$\frac{[CO][{H}_{2}]}{[C][{H}_{2}O]}$ | |
| D. | 增加C(s)的量,平衡正向移动 |
分析 A.正反应为吸热反应,升高体系温度,平衡正向移动,K增大;
B.平衡常数是温度的函数,与其他条件无关;
C.平衡常数表达式中固体和纯液体不代入表达式中;
D.固体物质的浓度视为定值,因此增加C(s)的量,平衡不移动.
解答 解:A.正反应为吸热反应,升高体系温度,平衡正向移动,K增大,故A错误;
B.化学平衡常数只受温度的影响,与体系的压强无关,故B正确;
C.C为固体,不带入K的表达式中,因此K=$\frac{c(CO)c({H}_{2})}{c({H}_{2}O)}$,故C错误;
D.固体物质的浓度视为定值,因此增加C(s)的量,平衡不移动,故D错误;
故选B.
点评 本题考查化学平衡影响因素、化学平衡常数,难度中等,注意掌握化学平衡常数的表达式的书写规则.

练习册系列答案
 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案
相关题目
20.下列有关说法中,正确的是( )
| A. | 乙醇和乙醚互为同分异构体 | |
| B. | 干馏煤可以得到甲烷、苯和氨等重要化工原料 | |
| C. | 乙醇和乙酸之间能发生酯化反应,酯化反应和皂化反应互为逆反应 | |
| D. | 在酸性条件下,蔗糖水解的化学方程式为 C12H22O11+H2O→2C6H12O6(葡萄糖) |
7.1L 0.1mol/L的AgNO3溶液在以Ag作阳极,Fe作阴极的电解槽中电解,当阴极上增重2.16g时,下列判断正确的是( )
| A. | 电解质AgNO3溶液的浓度变为0.08mol/L | |
| B. | 阳极上产生112mLO2(标况) | |
| C. | 转移1.204×1022个电子 | |
| D. | 反应中有0.01mol的Ag被氧化 |
17.下列有关有机物的实验操作、现象或结论不正确的是( )
| A. | 提纯含有杂质的工业乙醇,常用的方法是蒸馏 | |
| B. | 常温下,将二氧化碳通入苯酚钠溶液,溶液会变浑浊 | |
| C. | 混有泥沙的苯甲酸,除去杂质的方法是将其溶解后过滤,再蒸发结晶即可 | |
| D. | 苯和苯酚稀溶液分别与浓溴水混合,后者产生白色沉淀 |
4.将500mL pH=5的硫酸铜溶液(足量)用惰性电极电解一段时间,溶液pH变为2,若使溶液的浓度、pH与电解前相同,可采取的方法是( )
| A. | 向溶液中加入0.245g Cu(OH)2 | B. | 向溶液中加入0.31gCuCO3 | ||
| C. | 向溶液中加入0.0025 molH2SO4 | D. | 向溶液中加入0.2gCuO |
1.利用如图所示装置(电极均为惰性电极) 可吸收SO2,并制取硫酸和烧碱溶液,下列说法正确的是( )

| A. | 气体W为氧气 | |
| B. | b极与电源的正极相连 | |
| C. | 离子交换膜c为阳离子交换膜 | |
| D. | a极的电极反应为SO2+2H2O-2e-=SO42-+4H+. |
2.下列生活小常识或家庭小实验中不涉及化学变化的是( )
| A. | 用食醋去除水垢 | |
| B. | 用竹炭包可清楚衣柜内的异味 | |
| C. | 用铁钉等材料探究铁生锈的条件 | |
| D. | 用柠檬汁涂抹在切开苹果表面可防止苹果变色 |
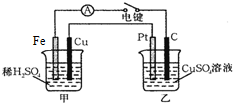 原电池和电解池都能实现能量的置换.回答下列问题:
原电池和电解池都能实现能量的置换.回答下列问题: