题目内容
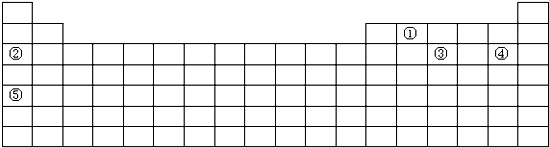
有A、B、C、D四种短周期元素,它们的原子序数由A到D依次增大,已知A和B原子有相同的电子层数,且A的L层电子数是K层电子数的两倍,C燃烧时呈现黄色火焰,C的单质在点燃条件下与B的单质充分反应,可以得到与D单质颜色相同的淡黄色固态化合物,试根据以上叙述回答:
(1)写出AB2的电子式为 .
(2)用电子式表示化合物C2D的形成过程 .
(1)写出AB2的电子式为
(2)用电子式表示化合物C2D的形成过程
考点:位置结构性质的相互关系应用
专题:
分析:有A、B、C、D四种短周期元素,它们的原子序数由A到D依次增大.已知A和B原子有相同的电子层数,则A、B处于同一周期,且A的L层电子数是K层电子数的两倍,则A有2个电子层,L层电子数为4,故A为碳元素;
C单质燃烧时呈现黄色火焰,则C为钠元素;C的单质在点燃时与足量的B单质充分反应,可以得到与D单质颜色相同的淡黄色固态化合物,则B为氧元素、D为硫元素,据此进行解答.
C单质燃烧时呈现黄色火焰,则C为钠元素;C的单质在点燃时与足量的B单质充分反应,可以得到与D单质颜色相同的淡黄色固态化合物,则B为氧元素、D为硫元素,据此进行解答.
解答:
解:有A、B、C、D四种短周期元素,它们的原子序数由A到D依次增大.已知A和B原子有相同的电子层数,则A、B处于同一周期,且A的L层电子数是K层电子数的两倍,则A有2个电子层,L层电子数为4,故A为碳元素;C单质燃烧时呈现黄色火焰,则C为钠元素;C的单质在点燃时与足量的B单质充分反应,可以得到与D单质颜色相同的淡黄色固态化合物,则B为氧元素,D为硫元素,
(1)CO2分子中碳原子与氧原子形成2对共用电子对,电子式为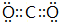 ,故答案为:
,故答案为: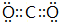 ;
;
(2)C2D是硫化钠,由钠离子与硫离子构成,硫化钠电子式为 ,用电子式表示其形成过程为:
,用电子式表示其形成过程为: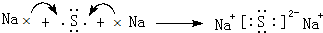 ,
,
故答案为: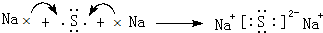 .
.
(1)CO2分子中碳原子与氧原子形成2对共用电子对,电子式为
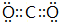 ,故答案为:
,故答案为: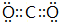 ;
;(2)C2D是硫化钠,由钠离子与硫离子构成,硫化钠电子式为
 ,用电子式表示其形成过程为:
,用电子式表示其形成过程为: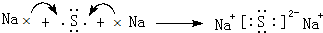 ,
,故答案为:
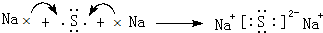 .
.
点评:本题考查结构性质位置关系应用,题目难度中等,正确推断各元素名称为解答关键,试题侧重对电子式的考查,注意掌握电子式表示化学键或物质的性质过程.

练习册系列答案
相关题目
某元素原子最外层只有1个电子,它跟卤素相结合时,所形成的化学键是( )
| A、一定形成共价键 |
| B、一定形成离子键 |
| C、可能形成共价键,也可能形成离子键 |
| D、以上说法都不对 |
将0.1mol两种气态烃组成的混合气体完全燃烧后得到3.36L(标准状况)CO2和3.6gH2O,下列说法正确的是( )
| A、一定有乙烯 |
| B、一定有甲烷 |
| C、一定没有甲烷 |
| D、一定没有乙烷 |
下列说法正确的是( )
| A、在中和热测定实验中,为准确测得反应前后的温差,应将已分别测得温度的氢氧化钠溶液与盐酸在隔热的容器中快速混合,并不断搅拌,用温度计测量混合液的最高温度 |
| B、往海带灰的浸泡液中加入过量的氯水,保证I-完全氧化为I2 |
| C、将溴乙烷与氢氧化钾混合液加热,再滴加硝酸银溶液,观察有淡黄色沉淀生成,可证明溴乙烷中含有溴 |
| D、润洗酸式滴定管时应从滴定管上口加入3~5mL所要盛装的酸溶液,倾斜着转动滴定管,使液体润湿其内壁,再从上口倒出,重复2~3次 |
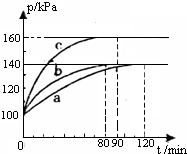 红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g),反应过程如下.
红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g),反应过程如下. 煤是重要的能,也是生产化工产品的重要原料.试用所学知识,解答下列问题:
煤是重要的能,也是生产化工产品的重要原料.试用所学知识,解答下列问题: