题目内容
18.如图是以氯化钠为例表示的氧化反应、还原反应,以及氧化还原反应实质的示意图.认真分析示意图,总结归纳:什么是氧化反应?什么是还原反应 氧化还原反应的实质是什么?氧化反应是失电子,化合价升高的反应;还原反应是得电子,化合价降低的反应;氧化还原反应的实质是电子的转移
分析 根据图示可以看出,氧化反应是失电子、化合价升高的反应,还原反应是得电子、化合价降低的反应,据此得出氧化还原反应的实质.
解答 解:根据图示可以看出,氧化反应是失电子,从而导致化合价升高的反应;还原反应是得电子,从而化合价降低的反应;故氧化还原反应的实质是电子的转移.故答案为:
氧化反应是失电子,化合价升高的反应;还原反应是得电子,化合价降低的反应;氧化还原反应的实质是电子的转移.
点评 本题通过图示可知氧化反应和还原反应以及氧化还原反应的实质,难度不大,注意基础的把握.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.下列各元素的氧化物中,既能与盐酸反应,又能与NaOH溶液反应的是( )
| A. | 元素X:原子中M层比L层少2个电子 | |
| B. | 元素Y:二价阳离子的核外电子总数与Ne原子相同 | |
| C. | 元素Z:K、L层电子总数是K、M层电子总数的2倍 | |
| D. | 元素W:该元素的某种氧化物能引起温室效应 |
13.在pH=1的溶液中,可以大量共存的离子是( )
| A. | K +、Na +、SO42-、S2O32- | B. | NH4+、Mg 2+、SO42-、Cl - | ||
| C. | Na +、K +、HCO3-、Cl - | D. | K +、Na +、AlO2-、NO3- |
3.利用下列各组物质制备和收集少量相应气体,能采用如图实验装置的是( )
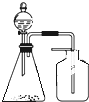

| A. | FeS与稀硫酸 | B. | 铜与浓硫酸 | C. | 稀硝酸与铜片 | D. | 电石与水 |
10.下列有关钠、铁、铝性质的说法中正确的是( )
| A. | 在地壳中的含量:Fe>Al>Na | |
| B. | 均能与盐酸反应,生成物中金属价态数值:Al>Fe>Na | |
| C. | 钠、铝均能从FeCl3溶液中置换出铁 | |
| D. | 等质量的三种金属与足量盐酸反应时,钠置换出的氢气最多 |
3.铬铁矿的主要成分可表示为FeO•Cr2O3,还含有MgO、Al2O3、Fe2O3等杂质,以下是以铬铁矿为原料制备重铬酸钾(K2Cr2O7)的流程图:

已知:①4FeO•Cr2O3+8Na2CO3+7O2$\stackrel{750℃}{→}$8Na2CrO4+2Fe2O3+8CO2↑;
②Na2CO3+Al2O3$\stackrel{750℃}{→}$2NaAlO2+CO2↑;③Cr2O72-+H2O 2CrO42-+2H+
根据题意回答下列问题:
(1)操作Ⅲ有多步组成,获得K2Cr2O7晶体的操作依次是:加入KCl固体、蒸发浓缩、冷却结晶、过滤、洗涤、干燥.
(2)酸化步骤用醋酸调节溶液pH<5,其目的是使CrO42-转化为Cr2O72-.
(3)固体X中主要含有Fe2O3、MgO(填写化学式);要检测酸化操作中溶液的pH是否等于4.5,应该使用pH计或精密pH试纸(填写仪器或试剂名称).如表是相关物质的溶解度数据,操作Ⅲ发生反应的化学方程式是:Na2Cr2O7+2KCl→K2Cr2O7↓+2NaCl.
(4)该反应在溶液中能发生的理由是K2Cr2O7的溶解度比Na2Cr2O7小(或四种物质中K2Cr2O7的溶解度最小).
(5)副产品Y主要含氢氧化铝,还含少量镁、铁的难溶化合物及可溶性杂质,精确分析Y中氢氧化铝含量的方法是称取n g样品,加入过量NaOH溶液(填写试剂)、溶解、过滤、再通入过量二氧化碳(填写试剂)、…灼烧、冷却、称量,得干燥固体m g.计算样品中氢氧化铝的质量分数为$\frac{26m}{17n}$(用含m、n的代数式表示).

已知:①4FeO•Cr2O3+8Na2CO3+7O2$\stackrel{750℃}{→}$8Na2CrO4+2Fe2O3+8CO2↑;
②Na2CO3+Al2O3$\stackrel{750℃}{→}$2NaAlO2+CO2↑;③Cr2O72-+H2O 2CrO42-+2H+
根据题意回答下列问题:
(1)操作Ⅲ有多步组成,获得K2Cr2O7晶体的操作依次是:加入KCl固体、蒸发浓缩、冷却结晶、过滤、洗涤、干燥.
(2)酸化步骤用醋酸调节溶液pH<5,其目的是使CrO42-转化为Cr2O72-.
(3)固体X中主要含有Fe2O3、MgO(填写化学式);要检测酸化操作中溶液的pH是否等于4.5,应该使用pH计或精密pH试纸(填写仪器或试剂名称).如表是相关物质的溶解度数据,操作Ⅲ发生反应的化学方程式是:Na2Cr2O7+2KCl→K2Cr2O7↓+2NaCl.
(4)该反应在溶液中能发生的理由是K2Cr2O7的溶解度比Na2Cr2O7小(或四种物质中K2Cr2O7的溶解度最小).
| 物质 | 溶解度/(g/100g水) | ||
| 0°C | 40°C | 80°C | |
| KCl | 28 | 40.1 | 51.3 |
| NaCl | 35.7 | 36.4 | 38 |
| K2Cr2O7 | 4.7 | 26.3 | 73 |
| Na2Cr2O7 | 163 | 215 | 376 |
4.称为“工业的血液”,以石油为原料不仅可以得到各种燃料油,还可以获得多种有机化工原料.请回答下列问题:
(1)将石蜡油与碎瓷片混合共热,产生的混合气体冷却至室温后,其成分如下:
(2)将2mol该混合气体通入足量的溴的四氯化碳溶液中,消耗Br2的物质的量为1mol.
(3)经发现,石蜡与碎瓷片混合共热的产物中,除气态烃CH4、C2H6、CH2═CH2外,还有另一种液态烃生成.0.2mol该液态烃在O2中完全燃烧时,得到的两种生成物的物质的量均为1.2mol,则该烃的分子式为C6H12.该烃的同分异构体有多种,其中一种的结构简式如图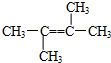 所示,
所示,
(4)该有机物分子中一定处于同一平面的碳原子数为6.
(1)将石蜡油与碎瓷片混合共热,产生的混合气体冷却至室温后,其成分如下:
| 物质 | CH4 | CH3-CH3 | CH2═CH2 |
| 物质的量分数 | 20% | 30% | 50% |
(3)经发现,石蜡与碎瓷片混合共热的产物中,除气态烃CH4、C2H6、CH2═CH2外,还有另一种液态烃生成.0.2mol该液态烃在O2中完全燃烧时,得到的两种生成物的物质的量均为1.2mol,则该烃的分子式为C6H12.该烃的同分异构体有多种,其中一种的结构简式如图
 所示,
所示,(4)该有机物分子中一定处于同一平面的碳原子数为6.
