题目内容
 下图为Fe(OH)2制备实验的改进装置,使用该装置将能在较长时间内观察到白色絮状沉淀.关于此实验,下列说法正确的是( )
下图为Fe(OH)2制备实验的改进装置,使用该装置将能在较长时间内观察到白色絮状沉淀.关于此实验,下列说法正确的是( )| A、装入药品后应关闭铁夹,等反应完成后再打开铁夹 |
| B、此装置是通过H2的排出使A中压强减小,从而将B中的烧碱吸入A中产生Fe(OH)2 |
| C、H2的作用是排尽装置内的空气和将A中溶液压人B中 |
| D、在药品用量上硫酸应过量,使铁粉能充分反应完 |
考点:制取氢氧化铁、氢氧化亚铁
专题:
分析:A.应该先打开止水夹,用生成的氢气将试管中空气排净,避免生成的氢氧化亚铁被空气中氧气氧化;
B.该装置时通过氢气产生的氢气使A中压强增大,从而将A中硫酸亚铁压入B中生成氢氧化亚铁;
C.该实验中,氢气的作用是排净装置中空气,然后将A中硫酸亚铁压入B中;
D.该实验中需要避免亚铁离子被氧化,最好铁粉应该过量,保证A中为硫酸亚铁.
B.该装置时通过氢气产生的氢气使A中压强增大,从而将A中硫酸亚铁压入B中生成氢氧化亚铁;
C.该实验中,氢气的作用是排净装置中空气,然后将A中硫酸亚铁压入B中;
D.该实验中需要避免亚铁离子被氧化,最好铁粉应该过量,保证A中为硫酸亚铁.
解答:
解:A.装入药品后应该打开止水夹,让铁与稀硫酸反应生成的氢气将装置中空气排净,避免后来生成的氢氧化亚铁被氧化,故A错误;
B.该装置是利用铁与稀硫酸反应生成的氢气将A中硫酸亚铁溶液压入B中,从而使硫酸亚铁与氢氧化钠溶液反应生成氢氧化亚铁,故B错误;
C.根据实验装置可知,本实验中氢气的作用有:先将装置中空气排净,然后关闭止水夹后将A中液体压入B中,故C正确;
D.亚铁离子易被氧化,为了避免硫酸亚铁被氧化,该实验中铁粉应该过量,故D错误;
故选C.
B.该装置是利用铁与稀硫酸反应生成的氢气将A中硫酸亚铁溶液压入B中,从而使硫酸亚铁与氢氧化钠溶液反应生成氢氧化亚铁,故B错误;
C.根据实验装置可知,本实验中氢气的作用有:先将装置中空气排净,然后关闭止水夹后将A中液体压入B中,故C正确;
D.亚铁离子易被氧化,为了避免硫酸亚铁被氧化,该实验中铁粉应该过量,故D错误;
故选C.
点评:本题考查了氢氧化亚铁的制备方法,题目难度中等,明确制备原理为解答关键,注意掌握氢氧化亚铁的性质及制备方法,试题培养了学生灵活应用基础知识的能力.

练习册系列答案
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案
相关题目
下列装置图正确的是( )
A、 容量瓶定容 |
B、 海水蒸馏原理 |
C、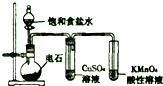 验证乙炔的性质 |
D、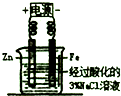 验证牺牲阳极的阴极保护法 |
化学与生活、生产密切相关,下列说法正确的是( )
| A、碳酸钡、碳酸氢钠、氢氧化铝均可作为抗酸药物使用 |
| B、人体内的蛋白质不断分解,最终生成水和二氧化碳排出体外 |
| C、工业生产玻璃和水泥,均需要用纯碱为原料 |
| D、“地沟油”的主要成分是油脂,其组成与汽油、煤油不相同 |
下列各组物质中,按单质、化合物、混合物顺序排序正确的是( )
| A、石墨、大理石、胆矾 |
| B、铁矿、小苏打、空气 |
| C、水银、水蒸气、氯水 |
| D、金属钠、食盐水、双氧水 |
短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示.下列说法正确的是( )
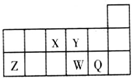

| A、原子半径Y<Z<W |
| B、元素Y的最高正化合价比元素X的最高正化合价高 |
| C、元素W的最高价氧化物对应的水化物的酸性比Q的弱 |
| D、元素X的气态氢化物的稳定性大于元素Y的气态氢化物的稳定性 |
若NA表示阿伏加德罗常数,下列说法正确的是( )
| A、在标准状况下,NA个水分子所占的体积约为22.4L |
| B、5.6g铁与氯气完全反应,失去电子的数目为0.2NA |
| C、足量Na与1molC12完全反应,转移的电子数为2NA |
| D、22.4L由N2、N2O组成的混合气体中所含有的氮原子的物质的量为2mol |
下列说法正确的是( )
A、已知X在一定条件下转化为Y, ,X与Y互为同分异构体,可用FeBr3溶液鉴别 ,X与Y互为同分异构体,可用FeBr3溶液鉴别 |
B、 能发生的反应类型有:加成反应、取代反应、消去反应、水解反应 能发生的反应类型有:加成反应、取代反应、消去反应、水解反应 |
| C、3-甲基-3-乙基戊烷的一氯取代产物有6种 |
| D、相同条件下乙酸乙酯在水中的溶解度比在乙醇中的溶解度要大 |
