题目内容
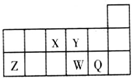
短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示.下列说法正确的是( )

| A、原子半径Y<Z<W |
| B、元素Y的最高正化合价比元素X的最高正化合价高 |
| C、元素W的最高价氧化物对应的水化物的酸性比Q的弱 |
| D、元素X的气态氢化物的稳定性大于元素Y的气态氢化物的稳定性 |
考点:元素周期律和元素周期表的综合应用
专题:
分析:根据X、Y、Z、W、Q所在周期表中的相对位置可知,X为N元素、Y为O元素、Z为Al元素、W为S元素、Q为Cl元素,再结合元素周期律的递变规律对各选项进行判断.
解答:
解:根据元素所在周期表中的位置可知,X为N元素、Y为O元素、Z为Al元素、W为S元素、Q为Cl元素,
A.原子核外电子层数越多,半径越大,同一周期元素原子半径从左到右逐渐减小,则原子半径大小为:Y<W<Z,故A错误;
B.Y为O元素,氧元素没有正化合价,X为N元素,N元素的最高正化合价为+5,故B错误;
C.金属性越强,最高价氧化物对应的水化物越强,非金属性:S<Cl,则最高价氧化物对应的水化物酸性强弱为:W<Q,故C正确;
D.非金属性越强,对应的气态氢化物温度下越强,非金属性:X<Y,则气态氢化物的稳定性:X<Y,故D错误;
故选C.
A.原子核外电子层数越多,半径越大,同一周期元素原子半径从左到右逐渐减小,则原子半径大小为:Y<W<Z,故A错误;
B.Y为O元素,氧元素没有正化合价,X为N元素,N元素的最高正化合价为+5,故B错误;
C.金属性越强,最高价氧化物对应的水化物越强,非金属性:S<Cl,则最高价氧化物对应的水化物酸性强弱为:W<Q,故C正确;
D.非金属性越强,对应的气态氢化物温度下越强,非金属性:X<Y,则气态氢化物的稳定性:X<Y,故D错误;
故选C.
点评:本题考查位置结构性质的相互关系及应用,为高频考点,题目难度中等,注意掌握元素周期表的结构和元素周期律的递变规律.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 下图为Fe(OH)2制备实验的改进装置,使用该装置将能在较长时间内观察到白色絮状沉淀.关于此实验,下列说法正确的是( )
下图为Fe(OH)2制备实验的改进装置,使用该装置将能在较长时间内观察到白色絮状沉淀.关于此实验,下列说法正确的是( )| A、装入药品后应关闭铁夹,等反应完成后再打开铁夹 |
| B、此装置是通过H2的排出使A中压强减小,从而将B中的烧碱吸入A中产生Fe(OH)2 |
| C、H2的作用是排尽装置内的空气和将A中溶液压人B中 |
| D、在药品用量上硫酸应过量,使铁粉能充分反应完 |
金属-硫电池价格低廉,使用寿命较长,能量密度高,因而在电池研究领域得到广泛关注.最近,我国科研工作者研究了一种能在室温下工作的新型Na-S电池.该电池放电过程的总反应方程式如下:nS+2Na=Na2Sn (注:能量密度指单位质量的电极材料可输出的电能,以W?h?kg-1为计量单位),则下列说法不正确的是( )
| A、该电池中用固态金属Na为负极,S单质作为正极,但S单质须负载在导电材料上 |
| B、该电池的电解质必须具备室温下传导Na+的能力,但不宜用NaOH溶液作为电解液 |
| C、n值越大则该电池的能量密度越高 |
| D、该电池充电过程中阳极的电极反应式:Na2Sn-2e-=2Na++nS,故充电时Na+从阳极向阴极迁移 |
据报导,我国某些城市的酸雨严重,为改变这一状况,某市正准备推广使用的清洁能源是( )
| A、太阳能 | B、石油 | C、水煤气 | D、煤 |
Al2O3MgO混合物溶于250mL盐酸得到无色溶液,逐滴加入0.5moL/LNaoH溶液,如图下列说法错误的是( )


| A、盐酸的物质的量浓度为0.22mol/L |
| B、混合物中Al2O3的物质的量为0.01mol |
| C、混合物中MgO的物质的量为0.01mol |
| D、P点加入NaOH溶液的体积是110mL |
下列说法不正确的是( )
A、 的分子式为C17H24O3 的分子式为C17H24O3 |
| B、水溶液中氨基酸在等电点时的溶解度最小.不同的氨基酸达到等电点的pH不同,故可以通过调节溶液pH分离某些氨基酸 |
C、有机硅聚醚( )可由单体 )可由单体  和 和 缩聚而成 缩聚而成 |
| D、等质量的甲醇、甲醛、甲醚完全燃烧时的耗氧量依次递增 |
 图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:
图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题: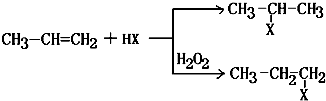 (X)为卤素原子
(X)为卤素原子 的物质,该物质是一种香料.
的物质,该物质是一种香料.