题目内容
15.设NA为阿伏伽德罗常数,下列说法中正确的是( )| A. | 含有1mol Na2SO4的溶液中,含有的Na+个数为NA | |
| B. | 18g水中含有电子数为8NA | |
| C. | 标准状况下,22.4LH2含有氢原子个数为2NA | |
| D. | 1.2L H2一定含有NA个氢原子 |
分析 A、Na2SO4含2个钠离子;
B、求出水的物质的量,然后根据1mol水中含10mol电子来分析;
C、求出氢气的物质的量,然后根据1mol氢气含2mol氢原子来计算;
D、氢气所处的状态不明确.
解答 解:A、Na2SO4含2个钠离子,故1molNa2SO4中含2mol钠离子,故A错误;
B、18g水的物质的量为1mol,而1mol水中含10mol电子,即10NA个,故B错误;
C、标况下,22.4L氢气的物质的量为1mol,而1mol氢气含2mol氢原子,即含2NA个氢原子,故C正确;
D、氢气所处的状态不明确,故1.2L氢气的物质的量不能计算,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
5.普通干电池两极材料是锌和石墨棒,两极间为MnO2、NH4Cl、ZnCl2糊状物,下列说法错误的是( )
| A. | 干电池中锌作负极,石墨棒作正极 | |
| B. | 负极发生还原反应:Zn-2e-═Zn2+ | |
| C. | MnO2的作用是把正极附近生成的氢气氧化成水,避免氢气泡出现 | |
| D. | 干电池工作时,由化学能转变为电能 |
6.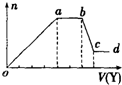 某无色稀溶液X中,可能含有下表所列离子中的某几种.现取该溶液适量,向其中加入某试剂Y,产生沉淀的物质的量(n)与加入试剂体积(V)的关系如图所示.
某无色稀溶液X中,可能含有下表所列离子中的某几种.现取该溶液适量,向其中加入某试剂Y,产生沉淀的物质的量(n)与加入试剂体积(V)的关系如图所示.
(1)若Y是盐酸,则X中一定含有的离子是CO32-、SiO32-、AlO2-、Na+,oa段发生反应的离子方程式SiO32-+2H+═H2SiO3↓、AlO2-+H++H2O═Al(OH)3↓,(指来源于X溶液的,下同) ab段发生反应的离子方程式CO32-+H+═HCO3-、HCO3-+H+═H2O+CO2↑,bc段发生反应的离子方程式Al(OH)3+3H+═Al3++3H2O.
(2)若Y是NaOH溶液,则X中一定含有的离子是Al3+、Mg2+、NH4+、Cl-,则oa段转化为沉淀的离子是Al3+、Mg2+,ab段反应的离子方程式为NH4++OH-═MH3•H2O.bc段反应的离子方程式为Al(OH)3+OH-═AlO2-+2H2O.
 某无色稀溶液X中,可能含有下表所列离子中的某几种.现取该溶液适量,向其中加入某试剂Y,产生沉淀的物质的量(n)与加入试剂体积(V)的关系如图所示.
某无色稀溶液X中,可能含有下表所列离子中的某几种.现取该溶液适量,向其中加入某试剂Y,产生沉淀的物质的量(n)与加入试剂体积(V)的关系如图所示.| 阴离子 | CO32-、Si32-、AlO2-、Cl- |
| 氧离子 | Al3+、Fe3+、Mg2+、NH4+、Na+ |
(2)若Y是NaOH溶液,则X中一定含有的离子是Al3+、Mg2+、NH4+、Cl-,则oa段转化为沉淀的离子是Al3+、Mg2+,ab段反应的离子方程式为NH4++OH-═MH3•H2O.bc段反应的离子方程式为Al(OH)3+OH-═AlO2-+2H2O.
3.N2中混有少量CO2气体和水蒸气,除去的正确操作是( )
| A. | 通过无水氯化钙的干燥管 | |
| B. | 通过浓硫酸的洗气瓶 | |
| C. | 先通过氢氧化钠溶液的洗气瓶,再通过浓硫酸的洗气瓶 | |
| D. | 先通过浓硫酸的洗气瓶,再通过氢氧化钠溶液的洗气瓶 |
10.气体摩尔体积在同温、同压下相等的本质原因是在同温、同压下( )
| A. | 气体体积的大小只随分子数变化 | |
| B. | 不同气体分子的大小几乎相等 | |
| C. | 不同气体分子间的平均距离几乎相等 | |
| D. | 气体分子的平均距离与分子本身大小成正比 |
20.下列各组混合物中,不能通过分液的方法进行分离的是( )
| A. | 酒精和水 | B. | 植物油和水 | C. | 汽油和水 | D. | 四氯化碳和水 |
7.下列有关实验操作的叙述中,错误的是( )
| A. | 实验室用排水集气法收集氧气完毕,把导管从水中取出,然后移去酒精灯 | |
| B. | 氢气还原氧化铜的实验结束,先移去酒精灯,待试管冷却后再停止通氢气 | |
| C. | 倾倒液体进行过滤时,应使液体沿着玻璃棒流下,且液面低于滤纸边缘 | |
| D. | 因NaOH有腐蚀性,可在天平两托盘上放同样的滤纸后再放NaOH,然后进行称量 |
4.给下列溶液中通入CO2气体,不可能产生沉淀的是( )
| A. | 氯化钙和硝酸钡的混合液 | B. | 稀的水玻璃 | ||
| C. | 偏铝酸钠溶液 | D. | 碳酸钠饱和溶液 |
5.某恒温密闭容器中,可逆反应A(s)?B+C(g)-Q达到平衡.缩小容器体积,重新达到平衡时,C(g)的浓度与缩小体积前的平衡浓度相等.以下分析正确的是( )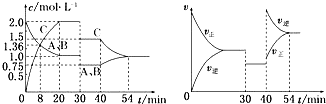

| A. | 产物B的状态只能为固态或液态 | |
| B. | 平衡时,单位时间内n(A)消耗:n(C)消耗=1:1 | |
| C. | 保持体积不变,向平衡体系中加入A,平衡向正反应方向移动 | |
| D. | 若开始时向容器中加入1 mol B和1 mol C,达到平衡时放出热量Q |