题目内容
14.下列有关氧元素及其化合物的表示或说法正确的是( )| A. | 氧原子的原子结构示意图: | |
| B. | 羟基的结构式:O-H | |
| C. | 用电子式表示Na2O的形成过程: | |
| D. | 组成为C2H6O的分子中可能只存在极性键 |
分析 A.O原子核内质子数为8,有2个电子层,最外层有6个电子;
B.羟基为中性原子团,羟基中含有1个氧氢键;
C.Na2O为离子化合物,根据离子化合物的电子式表示方法写出Na2O的形成过程;
D.不同非金属元素之间存在极性共价键.
解答 解:A.O原子核内质子数为8,有2个电子层,最外层有6个电子,原子结构示意图为: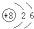 ,故A错误;
,故A错误;
B.羟基中含有1个氧氢键,羟基可以表示为-OH,故B错误;
C.Na2O为离子化合物,用电子式表示Na2O的形成过程为: ,故C错误;
,故C错误;
D.二甲醚只存在极性键,故D正确.
故选D.
点评 本题考查了常见化学用语的表示方法,题目难度中等,涉及结构式、原子结构示意图、形成过程、极性键等知识,注意熟练掌握常见化学用语的书写原则,试题培养了学生的灵活应用能力.

练习册系列答案
 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案
相关题目
5. 有机物X由C、H、O三种元素组成,其分子结构模型如图所示(图中球与球之间连线表示单键或双键).关于该有机物叙述正确的是( )
有机物X由C、H、O三种元素组成,其分子结构模型如图所示(图中球与球之间连线表示单键或双键).关于该有机物叙述正确的是( )
 有机物X由C、H、O三种元素组成,其分子结构模型如图所示(图中球与球之间连线表示单键或双键).关于该有机物叙述正确的是( )
有机物X由C、H、O三种元素组成,其分子结构模型如图所示(图中球与球之间连线表示单键或双键).关于该有机物叙述正确的是( )| A. | 分子中含有3种官能团 | |
| B. | 1 mol该有机物与足量溴水反应最多消耗3molBr2 | |
| C. | 1 mol该有机物最多能与2 mol NaOH反应 | |
| D. | 该有机物若能使酸性KMnO4溶液褪色,则可证明其分子中存在碳碳双键 |
9.下列实验方案、现象和结论均正确的是( )
| 选项 | A | B | C | D |
| 实验方案 | 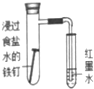 | 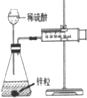 | 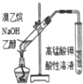 | 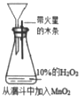 |
| 现象 | 导管中有红色柱 | 注射器的活塞往外推 | 高锰酸钾酸性溶液褪色 | 带火星的木条复燃 |
| 结论或作用 | 证明铁钉发生吸氧腐蚀 | 可用于测定反应物浓度对反应速率的影响 | 溴乙烷与NaOH乙醇溶液反应生成的气体是乙烯 | MnO2可与H2O2反应生成O2 |
| A. | A | B. | B | C. | C | D. | D |
19.根据元素周期律,由下列事实进行归纳推测,合理的是( )
| 事实 | 推测 | |
| A | Mg与水反应缓慢,Ca与水反应较快 | Be与水反应会更快 |
| B | HCl在1500℃时分解,HI在230℃时分解 | HBr的分解温度介于二者之间 |
| C | SiH4,PH3在空气中能自燃 | H2S在空气中也能自燃 |
| D | 标况下HCl,HBr均为气体 | HF也为气体 |
| A. | A | B. | B | C. | C | D. | D |
6.某固体混合物可能由Al、(NH4)2SO4、MgCl2、FeCl2、AlCl3中的两种或多种组成,现对该混合物做如下实验,现象和有关数据如图所示(气体体积数据已换算成标准状况).关于该固体混合物,下列说法正确的是( )


| A. | 含4.5gAl | |
| B. | 一定不含FeCl2,可能含有MgCl2和AlCl3 | |
| C. | 含有物质的量相等的(NH4)2SO4和MgCl2 | |
| D. | 含有MgCl2和FeCl2 |
3.下列说法正确的是( )
| A. | 油脂在NaOH热溶液中完全水解后,加入热饱和食盐水可观察到液面上有固体析出 | |
| B. | 容量瓶、滴定管和分液漏斗均标有“O”刻度线,使用前均需要检漏 | |
| C. | 实验室用二氧化锰与浓盐酸制氯气时,先加热二氧化锰再滴加浓盐酸 | |
| D. | 为检验摩尔盐中的NH4+,可向试样加入少量的稀Na0H,再用pH试纸检验 |
4.化学深入我们生活,下列说法不正确的是( )
| A. | 食盐可做食物调味剂,也可做食品防腐剂 | |
| B. | 高锰酸钾溶液、酒精、双氧水都能杀菌消毒,都利用了强氧化性 | |
| C. | 海水淡化的方法主要有蒸馏法、离子交换法等 | |
| D. | 通常所说的三大合成材料是指塑料、合成橡胶和合成纤维 |

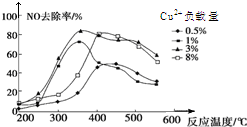 雾霾严重影响人们的生活,汽车尾气的排放是造成雾霾天气的重要原因之一.已知汽车尾气排放时容易发生以下反应:
雾霾严重影响人们的生活,汽车尾气的排放是造成雾霾天气的重要原因之一.已知汽车尾气排放时容易发生以下反应: